Hvordan kemiske bindinger brydes og reformeres:Videnskaben om endoterme og eksoterme reaktioner
blanscape/iStock/GettyImages
I hver kemisk reaktion spaltes etablerede molekylære bindinger, mens nye bindinger dannes. Almindelige eksempler omfatter forbrænding, reduktion og nedbør. Omlejringen af atomer giver helt nye forbindelser. Mens blot kontakt mellem reaktanter kan være tilstrækkelig, kræver de fleste reaktioner en ekstern trigger - typisk varme - for at starte bindingsspaltning. Resultatet afhænger af samspillet mellem molekylære kræfter, energitilstande og miljøforhold.
TL;DR (for lang; læste ikke)
Kemiske reaktioner danner og bryder bindingerne mellem molekyler og producerer nye materialer. De kan opstå spontant eller har brug for energitilførsel. At bryde bindinger absorberer energi; dannelse af bindinger frigiver energi, så den samlede reaktion kan være endoterm eller eksoterm.
Kemiske bindinger og energiniveauer
Grundlaget for kemi er nedbrydning (nedbrydning) og dannelse (syntese) af bindinger. Nedbrydning er endoterm, fordi stabile bindinger skal overvindes ved energitilførsel. Omvendt er syntese eksoterm; atomer når en mere stabil konfiguration med lavere energi og frigiver energi. En reaktions nettoenergiændring afhænger af balancen mellem bindingsspaltning og bindingsdannelse.
For eksempel får opvarmning af kviksølv(II)oxid (√HgO) det til at nedbrydes til kviksølvmetal og oxygengas og absorberer varme i processen.
Endotermiske reaktioner
Endoterme reaktioner kræver en energitilførsel for at bryde bindinger og igangsætte processen. De opstår sjældent spontant. Et eksempel er den termiske nedbrydning af kviksølv(II)oxid, som kræver varme for at fortsætte. Mere komplekse endoterme reaktioner kan trække varme fra deres omgivelser; faststofreaktionen mellem bariumhydroxid og ammoniumchlorid ved stuetemperatur producerer bariumchlorid og ammoniak, mens blandingen afkøles og absorberer varme fra beholderen og den omgivende luft.
Eksotermiske reaktioner
Eksoterme reaktioner frigiver varme og er ofte selvbærende. Syntesereaktioner, såsom den kraftige reaktion af natrium med vand, genererer natriumhydroxid og brintgas, mens de producerer nok varme til at antænde brinten. Forbrænding af kulbrinter - træ, benzin eller brændselsolie - kræver en indledende gnist eller flamme for at bryde nogle få bindinger. Når først de nye, energetisk gunstige bindinger dannes, holder den frigivne varme reaktionen i gang og producerer kuldioxid og vanddamp.
Industrielle og kommercielle processer udnytter ofte eksoterme, selvopretholdende reaktioner. Deres effektivitet og det arbejde, de leverer, afhænger af de specifikke reaktanter og de bindinger, der brydes og omdannes under reaktionen.
 Varme artikler
Varme artikler
-
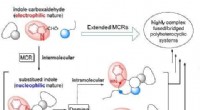 Nye multikomponentreaktionsgrænserEksperterne skaber et hovedprincip, hvormed polaritetsændringen af en reaktiv i en multikomponentproces afkæder domino -reaktioner. Kredit:Angewandte Chemie International Edition Syntesen af k
Nye multikomponentreaktionsgrænserEksperterne skaber et hovedprincip, hvormed polaritetsændringen af en reaktiv i en multikomponentproces afkæder domino -reaktioner. Kredit:Angewandte Chemie International Edition Syntesen af k -
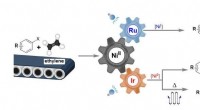 Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere
Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere -
 Billig detektor er som velcro til kræftcellerKredit:American Chemical Society Forskere har udviklet en ny type sensor, der fungerer som velcro for prostatacancerceller, klæbe dem på et modificeret matglas, som dem, der bruges i naturfag, så
Billig detektor er som velcro til kræftcellerKredit:American Chemical Society Forskere har udviklet en ny type sensor, der fungerer som velcro for prostatacancerceller, klæbe dem på et modificeret matglas, som dem, der bruges i naturfag, så -
 At finde generne til at bygge en bedre kræftbehandlingPacific Yew bark. Kredit:Walter Siegmund / Wikimedia / CC BY 2.5 Forskere er et skridt tættere på at forstå, hvordan det kræftbekæmpende stof Taxol produceres af træer. I en nylig artikel offentl
At finde generne til at bygge en bedre kræftbehandlingPacific Yew bark. Kredit:Walter Siegmund / Wikimedia / CC BY 2.5 Forskere er et skridt tættere på at forstå, hvordan det kræftbekæmpende stof Taxol produceres af træer. I en nylig artikel offentl


