Rubidium- og klorreaktion:Produkter og mekanisme
Reaktion:
2 Rb (s) + Cl2 (g) → 2 RbCl (s)
Forklaring:
* Rubidium har en valenselektron og mister den let for at opnå en stabil elektronkonfiguration. Det danner en +1-kation (Rb+).
* Klor har syv valenselektroner og får let en elektron for at opnå en stabil elektronkonfiguration. Det danner en -1 anion (Cl⁻).
* Elektrostatisk tiltrækning mellem de positivt ladede rubidiumioner og de negativt ladede chloridioner danner en ionbinding.
* Den resulterende forbindelse, rubidiumchlorid , er et hvidt krystallinsk fast stof, der er meget opløseligt i vand.
Egenskaber af rubidiumchlorid:
* Hvidt krystallinsk fast stof
* Meget opløseligt i vand
* Smeltepunkt:718°C
* Kogepunkt:1390°C
* Bruges i forskellige applikationer, herunder:
* Produktion af andre rubidiumforbindelser
* Forskning og udvikling
* Optiske fibre
Vigtig bemærkning: Reaktionen mellem rubidium og klor er meget eksoterm, hvilket betyder, at den frigiver en betydelig mængde varme. Reaktionen skal udføres med forsigtighed og passende sikkerhedsforanstaltninger.
Sidste artikelArsen Pentachlorid (AsCl₅) Hybridisering:Forstå sp³d²
Næste artikelBeregning af oxidationstallet for kulstof i C₂O₄²⁻
 Varme artikler
Varme artikler
-
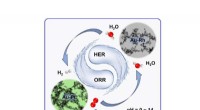 Kemikere udvikler ædelmetal -aerogeler til elektrokemisk brintproduktionNy ædelmetal-aerogeler blev udviklet til fremragende pH-universel elektrokatalyse mod hydrogenudviklingsreaktion og iltreduktionsreaktion. Kredit:Wiley-VCH Elektrocatalyse er et af de mest studere
Kemikere udvikler ædelmetal -aerogeler til elektrokemisk brintproduktionNy ædelmetal-aerogeler blev udviklet til fremragende pH-universel elektrokatalyse mod hydrogenudviklingsreaktion og iltreduktionsreaktion. Kredit:Wiley-VCH Elektrocatalyse er et af de mest studere -
 Teknologisk stråle af håb for snowboardscenenJakob Schmidt og Marc Fleischmann, forskningsassistenter ved Institut for Tekstilteknologier ved Chemnitz University of Technology, kontrollere kvaliteten af et splitboards præform på pladespilleren
Teknologisk stråle af håb for snowboardscenenJakob Schmidt og Marc Fleischmann, forskningsassistenter ved Institut for Tekstilteknologier ved Chemnitz University of Technology, kontrollere kvaliteten af et splitboards præform på pladespilleren -
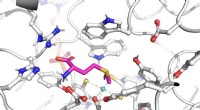 Små forskelle i aminosyrer kan føre til dramatisk forskellige enzymerKredit:University of Queensland Blot nogle få ændringer af et enzyms aminosyrer kan være nok til dramatisk at ændre dets funktion, gør det muligt for mikrober at leve i vildt forskellige miljøer.
Små forskelle i aminosyrer kan føre til dramatisk forskellige enzymerKredit:University of Queensland Blot nogle få ændringer af et enzyms aminosyrer kan være nok til dramatisk at ændre dets funktion, gør det muligt for mikrober at leve i vildt forskellige miljøer. -
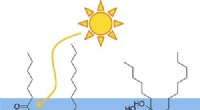 De radikale måder, hvorpå sollys bygger større molekyler i atmosfærenKredit:American Chemical Society Med sommeren nærmer sig, hav og sol kan måske fremtrylle billeder af en strandtur. Men for videnskabsmænd, samspillet mellem de to har store konsekvenser for klima
De radikale måder, hvorpå sollys bygger større molekyler i atmosfærenKredit:American Chemical Society Med sommeren nærmer sig, hav og sol kan måske fremtrylle billeder af en strandtur. Men for videnskabsmænd, samspillet mellem de to har store konsekvenser for klima
- Flyder alle geodes i vand?
- Hvad spiser Rosellas?
- Den monomer, der er ansvarlig for dannelsen af sulfidbindinger i polypeptider, er?
- Hvordan er tryk involveret i smeltende mantelmateriale ved en mid-ocean ryg?
- Hvor mange mol aluminiumoxid er i 12,75 g aluminiumoxidened at vide?
- 3-D print, biologiforskning tager turen tilbage til jorden ombord på SpaceXs Dragon


