Kovalent binding:Opfører elektroner sig identisk?
Her er det korte svar:
Elektronerne involveret i kovalent binding er ikke identiske i den forstand, at de har unikke individuelle identiteter. Men de opfører sig som om de var identiske , hvilket betyder, at de deles ligeligt mellem atomerne i bindingen.
Her er grunden:
* Kvantemekanik: Elektroner er styret af kvantemekanikkens love, hvor de eksisterer som sandsynlighedsskyer snarere end særskilte partikler med bestemte placeringer. I en kovalent binding overlapper de deltagende atomers elektronskyer og blander sig, hvilket skaber en ny, fælles elektronsky.
* Lige deling: På grund af elektronskyens fælles natur er elektronerne stort set ikke til at skelne. Der er ingen måde at sige, hvilken elektron der kom fra hvilket atom. De bliver "delokaliserede" over hele obligationen.
* Symmetri: I en symmetrisk kovalent binding (som H2) er deling af elektroner helt ens. I asymmetriske bindinger (som H-Cl) er elektronerne stadig delt, men de kan bruge mere tid tættere på det ene atom end det andet.
Opsummering: Mens elektronerne involveret i kovalent binding ikke virkelig er identiske i den forstand, at de har individuelle identiteter, opfører de sig, som om de var identiske, hvilket skaber en delt elektronsky, der binder atomerne sammen.
Sidste artikelJernrust:Hvad er det, og hvordan dannes det?
Næste artikelForstå den molekylære struktur af salt (NaCl)
 Varme artikler
Varme artikler
-
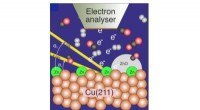 Forskere optrævler den aktive fase i katalytisk kuldioxidreduktion til methanolFigur illustrerer en Cu-overflade dækket med en lille mængde Zn, der er probet med fotoelektronspektroskopi under reaktion af CO2, CO og H2 til methanol. Kredit:Stockholm Universitet Forskere ved S
Forskere optrævler den aktive fase i katalytisk kuldioxidreduktion til methanolFigur illustrerer en Cu-overflade dækket med en lille mængde Zn, der er probet med fotoelektronspektroskopi under reaktion af CO2, CO og H2 til methanol. Kredit:Stockholm Universitet Forskere ved S -
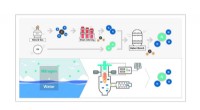 Den nye alkymi i kulstofneutralitet:At forvandle vand til ammoniak med kun vedvarende energi(Øverst) Harber-Bosch-metoden:brug af brint (ekstraheret ved termisk nedbrydning af naturgas) og atmosfærisk nitrogen som reaktanter, denne metode producerer ammoniak ved anvendelse af katalysator und
Den nye alkymi i kulstofneutralitet:At forvandle vand til ammoniak med kun vedvarende energi(Øverst) Harber-Bosch-metoden:brug af brint (ekstraheret ved termisk nedbrydning af naturgas) og atmosfærisk nitrogen som reaktanter, denne metode producerer ammoniak ved anvendelse af katalysator und -
 Forskere opnår termokemiluminescens i fast tilstand med krystallerFaststof termokemiluminescens af krystaller, der udsender lys, når de opvarmes, optaget af NYUAD-forskere. Kredit:Dr. Stefan Schramm Fundene, offentliggjort i tidsskriftet Naturkommunikation , d
Forskere opnår termokemiluminescens i fast tilstand med krystallerFaststof termokemiluminescens af krystaller, der udsender lys, når de opvarmes, optaget af NYUAD-forskere. Kredit:Dr. Stefan Schramm Fundene, offentliggjort i tidsskriftet Naturkommunikation , d -
 Miljøpåvirkning af frostvæske:Virkninger på dyreliv, planter og jordHvad er frostvæske? Frostvæske er en væske, der sænker vandets frysepunkt og beskytter motorens kølesystemer mod frostskader og overkogning. Det er typisk en blanding af vand og en glykol, sædvanligv
Miljøpåvirkning af frostvæske:Virkninger på dyreliv, planter og jordHvad er frostvæske? Frostvæske er en væske, der sænker vandets frysepunkt og beskytter motorens kølesystemer mod frostskader og overkogning. Det er typisk en blanding af vand og en glykol, sædvanligv
- Familieseksualundervisning blandt anden generation af sydasiatiske amerikanske studerende
- Bruges til at demonstrere jordens rotation?
- Mestring af forhold og proportioner:En praktisk guide til matematiske beregninger
- En transformativ metasurface baseret på en zerogap-indlejret skabelon
- Hvordan konverterer jeg M3 til kilogram?
- Hvordan adskiller du jernfyldninger fra svovl?


