Lewis-struktur af P₄O₁₀:En trin-for-trin guide
1. Tæl valenselektroner:
* Fosfor (P) har 5 valenselektroner, og der er 4 fosforatomer, så 5 * 4 =20 elektroner.
* Ilt (O) har 6 valenselektroner, og der er 10 iltatomer, så 6 * 10 =60 elektroner.
* Samlet valenselektroner:20 + 60 =80 elektroner
2. Bestem det eller de centrale atomer:
* Fosfor er mindre elektronegativt end oxygen, så det vil være det centrale atom.
3. Forbind atomerne med enkeltbindinger:
* Forbind de fire fosforatomer i en tetraedrisk form.
* Forbind hvert fosforatom til tre oxygenatomer.
4. Fordel resterende elektroner:
* Du har brugt 12 enkeltbindinger (12 * 2 =24 elektroner), hvilket efterlader 56 elektroner.
* Placer ensomme par på hvert oxygenatom for at fuldende deres oktetter (8 elektroner omkring hver oxygen). Du skal bruge 48 elektroner til dette.
* Placer de resterende 8 elektroner som enlige par på fosforatomerne.
5. Tjek formelle gebyrer:
* Den formelle ladning på hvert atom bør minimeres. Fosforatomerne vil have en formel +1 ladning, og oxygenatomerne med enkeltbindinger vil have en formel -1 ladning. Oxygenatomerne med dobbeltbindinger vil have en formel 0-ladning.
Endelig struktur:
Lewis-strukturen af P4O10 vil have:
* Fire centrale fosforatomer arrangeret i en tetraedrisk form.
* Hvert fosforatom er forbundet med tre oxygenatomer.
* To af oxygenatomerne forbundet med hvert fosforatom er forbundet med dobbeltbindinger, og det ene er forbundet med en enkeltbinding.
* Hvert oxygenatom vil have to ensomme elektronpar.
* Hvert fosforatom vil have ét ensomt elektronpar.
Vigtig bemærkning: Mens Lewis-strukturen hjælper med at visualisere bindingen, har P4O10 en mere kompleks 3D-struktur, hvor phosphoratomerne danner et tetraeder, og oxygenatomerne danner bro mellem dem.
 Varme artikler
Varme artikler
-
 Røntgenbilleder af menneskeskalle for at forbedre militærhjelmeKredit:CC0 Public Domain Forskere bruger ofte komplekse computermodeller af kraniet og hjernen, når de designer hjelme for at forhindre eller minimere skader på hovedet på grund af stød. Disse mod
Røntgenbilleder af menneskeskalle for at forbedre militærhjelmeKredit:CC0 Public Domain Forskere bruger ofte komplekse computermodeller af kraniet og hjernen, når de designer hjelme for at forhindre eller minimere skader på hovedet på grund af stød. Disse mod -
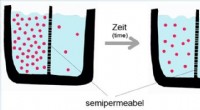 Forstå diffusion:Hvordan molekyler bevæger sig fra høj til lav koncentrationAf bidragyder | Opdateret 24. marts 2022 Diffusion forklaret Diffusion er den spontane bevægelse af molekyler fra et område med højere koncentration til et område med lavere koncentration, drevet af
Forstå diffusion:Hvordan molekyler bevæger sig fra høj til lav koncentrationAf bidragyder | Opdateret 24. marts 2022 Diffusion forklaret Diffusion er den spontane bevægelse af molekyler fra et område med højere koncentration til et område med lavere koncentration, drevet af -
 Kalorimeterkonstant:Trin-for-trin kalibreringsvejledningAf John Brennan | Opdateret 30. august 2022 Oversigt Kalorimetre kvantificerer varmeændringen i kemiske reaktioner eller fysiske transformationer, såsom issmeltning. At kende kalorimeterkonstanten er
Kalorimeterkonstant:Trin-for-trin kalibreringsvejledningAf John Brennan | Opdateret 30. august 2022 Oversigt Kalorimetre kvantificerer varmeændringen i kemiske reaktioner eller fysiske transformationer, såsom issmeltning. At kende kalorimeterkonstanten er -
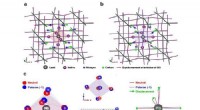 Skinner lys over spændingstilstande i perovskitmaterialerTeoretisk forudsagte strukturer af MAPbI 3 hybrid perovskit:en neutral klynge. b negativt ladet (polaron) klynge. c Forskellige perspektivlige sammenligninger af den neutrale (røde sfære) og polaron
Skinner lys over spændingstilstande i perovskitmaterialerTeoretisk forudsagte strukturer af MAPbI 3 hybrid perovskit:en neutral klynge. b negativt ladet (polaron) klynge. c Forskellige perspektivlige sammenligninger af den neutrale (røde sfære) og polaron


