Beregning af atomer:Hvor mange atomer i 5,22 g fosfor?
1. Find den molære masse af fosfor:
* Den molære masse af fosfor (P) er cirka 30,97 g/mol.
2. Beregn antallet af mol fosfor:
* Divider massen af fosfor med dens molære masse:
* mol P =5,22 g / 30,97 g/mol =0,168 mol
3. Brug Avogadros tal til at finde antallet af atomer:
* Avogadros tal er 6,022 x 10^23 atomer/mol.
* Gang antallet af mol med Avogadros tal:
* antal atomer =0,168 mol * 6,022 x 10^23 atomer/mol
* antal atomer ≈ 1,01 x 10^23 atomer
Derfor er der ca. 1,01 x 10^23 atomer i 5,22 g fosfor.
Sidste artikelAluminium og saltsyrereaktion:ligning og forklaring
Næste artikelLewis-struktur af P₄O₁₀:En trin-for-trin guide
 Varme artikler
Varme artikler
-
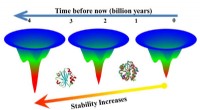 Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv
Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv -
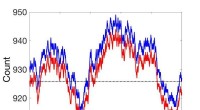 Ikke-steady state massehandlingsdynamik genovervejetSammenligninger mellem ikke-steady state stokastiske kinetiske simuleringer (rød) og simuleringer ved brug af koblet reaktionssætning (blå). Kredit:Pacific Northwest National Laboratory Masseaktio
Ikke-steady state massehandlingsdynamik genovervejetSammenligninger mellem ikke-steady state stokastiske kinetiske simuleringer (rød) og simuleringer ved brug af koblet reaktionssætning (blå). Kredit:Pacific Northwest National Laboratory Masseaktio -
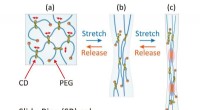 Biokompatible hydrogelmaterialer kan hurtigt komme sig efter mekanisk belastningEn strain gauge trækker prøver af hydrogel fra hinanden. (Øvre) En typisk gel med et hak skåret i venstre side snappede kort tid efter at den var strakt. (Midt) Den nye selvforstærkede gel havde et ha
Biokompatible hydrogelmaterialer kan hurtigt komme sig efter mekanisk belastningEn strain gauge trækker prøver af hydrogel fra hinanden. (Øvre) En typisk gel med et hak skåret i venstre side snappede kort tid efter at den var strakt. (Midt) Den nye selvforstærkede gel havde et ha -
 Højtliggende fugle udvikler lignende egenskaber via forskellige mutationerEn gengivelse af aviær hæmoglobin, blodproteinet, der fanger og leverer ilt i hele kroppen. Kredit:Proceedings of the National Academy of Sciences USA På det tibetanske plateau i Himalaya og Altip
Højtliggende fugle udvikler lignende egenskaber via forskellige mutationerEn gengivelse af aviær hæmoglobin, blodproteinet, der fanger og leverer ilt i hele kroppen. Kredit:Proceedings of the National Academy of Sciences USA På det tibetanske plateau i Himalaya og Altip
- Hvordan varierer resistens af metal med temperatur?
- Hvilken stjerne er objektet, der fortsætter med at skinne svagt i milliarder af år, da det langsom…
- Metabolisme påvirker direkte chancerne for at udvikle malaria
- En type M -stjerne vises sandsynligvis?
- Søger ud over grafen efter nye vidundermaterialer
- Hvad er ladningen af kobberion og sulfat i CuSo4?


