Kalorimeterkonstant:Trin-for-trin kalibreringsvejledning
Af John Brennan | Opdateret 30. august 2022
Oversigt
Kalorimetre kvantificerer varmeændringen i kemiske reaktioner eller fysiske transformationer, såsom issmeltning. At kende kalorimeterkonstanten er afgørende for at konvertere temperaturændringer til energiværdier og for nøjagtig fortolkning af reaktionens termodynamik. Denne guide guider dig gennem en praktisk, reproducerbar metode til kalibrering af et simpelt kaffekopkalorimeter.
Sikkerhedsforanstaltninger
- Bær en laboratoriefrakke, beskyttelsesbriller og handsker.
- Placer aldrig hår, tøj eller brændbare materialer i nærheden af åben ild.
- Håndter varmt vand (≈80°C) forsigtigt for at undgå forbrændinger.
Materialer
- Kaffekopkalorimeter (to Styrofoam-kopper, låg, termometer)
- To digitale termometre eller kviksølvtermometre
- Bunsenbrænder, lighter, ringstand, klemme, trådgaze
- Tørt 150 ml bægerglas
- Skaler nøjagtigt til 0,01 g
- Klassificeret cylinder
- Regnearkssoftware (Excel, OpenOffice Calc)
- Lommeregner
- Vand (stuetemperatur og varmt)
- Laboratoriefrakke, beskyttelsesbriller, handsker
Procedure
- Saml kalorimeteret. Sæt den ene Styrofoam-kop i den anden, fastgør låget, og anbring et termometer i koppen gennem et lille hul i låget.
- Vej det tomme kalorimeter. Optag massen til nærmeste 0,01 g.
- Tilsæt 50 ml koldt vand. Brug en gradueret cylinder; præcis volumen er ikke kritisk på dette stadium. Genvej kalorimeteret, og beregn vandmassen ud fra vægtforskellen.
- Væg bægeret. Optag dens masse. Tilsæt 50mL vand, genvej og beregn massen af det varme vand.
- Opvarm vandet. Placer bægerglasset på trådnet over Bunsen-brænderen, indsæt et termometer, og opvarm forsigtigt til ≈80°C, undgå hurtig kogning.
- Rør i kalorimeteret. Brug en klemme, suspender det andet termometer i det kolde vand og omrør i fire minutter. Optag temperatur hvert minut; værdien skal være stabil.
- Overfør varmt vand. Sluk for brænderen i det fjerde minut, noter varmtvandstemperaturen og hæld det i kalorimeteret. Sæt låget på igen, og genoptag omrøringen.
- Optag temperatur. Mål kalorimetertemperaturen hvert 30. sekund i de næste fem minutter.
- Analyser data. Importer tids- og temperaturdata til et regneark. Plot efterblandingstemperaturerne (ekskluder forblandingspunkter), og tilpas en lineær trendlinje.
- Ekstrapoler sluttemperaturen. Brug linjen med bedst tilpasning til at estimere temperaturen til 5 minutter (Tf).
- Beregn temperaturændringer.
- Varmtvandsskift (ΔTh) =indledende varmtvandstemperatur – Tf.
- Koldvandsændring (ΔTc) =Tf – indledende koldtvandstemperatur.
- Beregn energiændringer.
- Energi tabt af varmt vand:Qh =mh × 4,184Jg⁻¹°C⁻¹ × ΔTh.
- Energi opnået af koldt vand:Qc =mc × 4,184Jg⁻¹°C⁻¹ × ΔTc.
- Bestem kalorimeterets energi. Qcal =Qh – Qc.
- Beregn konstant. Ckal =Qcal / ΔTc. Resultatet, udtrykt i J°C⁻¹, er kalorimeterkonstanten.
Vigtige bemærkninger
- Konstanten skal være positiv; en negativ værdi angiver en procedurefejl.
- Gentag kalibreringen flere gange, og gennemsnit resultaterne for at minimere tilfældige fejl.
- Rapportér det endelige gennemsnit ±2σ, hvor σ er standardafvigelsen for forsøgene.
Referencer
- Atkins, P., &Jones, L. (2008). Kemiske principper:The Quest for Insight, 4. udgave .
- Berniolles, S. (2011). Chemistry 7L Lab Manual .
Sidste artikelHvordan opløselighed kvantificeres:enheder og definitioner
Næste artikelTrin-for-trin guide til løsning af titreringsproblemer
 Varme artikler
Varme artikler
-
 Mediciner 3D-printet på syv sekunderKredit:University College London Medicin kan printes på syv sekunder i en ny 3D-printteknik, der kan muliggøre hurtig on-site produktion af medicin, rapporterer et UCL-ledet forskerhold. Resultate
Mediciner 3D-printet på syv sekunderKredit:University College London Medicin kan printes på syv sekunder i en ny 3D-printteknik, der kan muliggøre hurtig on-site produktion af medicin, rapporterer et UCL-ledet forskerhold. Resultate -
 Upcycling af plastikflasker kunne give dem et mere nyttigt andet livDisse kompositmaterialer, udviklet af upcycling af PET, kan bruges i vindmøller, snowboards, eller materialer som ballistisk nylon og genanvendelige flasker, der kan bruges flere gange, før de genbrug
Upcycling af plastikflasker kunne give dem et mere nyttigt andet livDisse kompositmaterialer, udviklet af upcycling af PET, kan bruges i vindmøller, snowboards, eller materialer som ballistisk nylon og genanvendelige flasker, der kan bruges flere gange, før de genbrug -
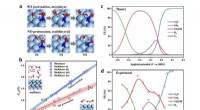 Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid (
Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid ( -
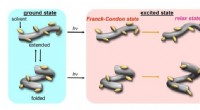 Under tryk:Manipulering af protein-efterlignende molekyler med hydrostatisk trykI grundtilstanden, værten vedtager to konformere, en forlænget og en foldet, og gradvist skifter til en udvidet-rig tilstand efter tryk. Derefter, i ophidset tilstand (hυ), disse to konformere udsende
Under tryk:Manipulering af protein-efterlignende molekyler med hydrostatisk trykI grundtilstanden, værten vedtager to konformere, en forlænget og en foldet, og gradvist skifter til en udvidet-rig tilstand efter tryk. Derefter, i ophidset tilstand (hυ), disse to konformere udsende
- Er kropsvægt mest påvirket af miljøet?
- Hvad var Ernest største bidrag til kemi?
- Hvad er et fossilt brændstof, og hvordan fremstilles de?
- Hvordan bliver bakterier egentlig resistente over for antibiotika?
- Hvad kan helium gøre?
- Hvorfor New York City er gennemsnitligt:Forskere ønsker at forbedre, hvordan vi bestemmer urban e…


