Trin-for-trin guide til løsning af titreringsproblemer
Af John Brennan • Opdateret 30. august 2022
Når kemikere skal bestemme koncentrationen af en opløst art, anvender de typisk titrering. Ved at tilføje et reagens, der reagerer kvantitativt med analytten, indtil reaktionen når ækvivalenspunktet, kan kemikeren tilbageberegne den oprindelige koncentration.
Trin 1:Identificer syre- eller basestyrke
Bestem, om analytten og titranten er stærk eller svag. En stærk syre donerer fuldt ud protoner; en stærk base accepterer dem fuldt ud. Almindelige stærke syrer omfatter HCl, HNO3, H2SO4, HClO4, HBr og HI. Stærke baser omfatter LiOH, NaOH, KOH, RbOH, Ca(OH)2, Sr(OH)2 og Ba(OH)2. Se den fulde liste over almindelige syrer og baser.
Trin 2:Forudsig saltets natur
Når en stærk syre reagerer med en stærk base, er det resulterende salt neutralt (pH≈7). En stærk syre med en svag base giver et surt salt; en stærk base med en svag syre giver et basisk salt. Titreringer parrer sjældent to svage arter, fordi det bliver udfordrende at lokalisere ækvivalenspunktet.
Trin 3:Klargør problemformuleringen
Angiv de kendte mængder:identiteter af analyt og titrant, analytvolumen, titrantkoncentration og eventuelle givne mol eller volumener ved ækvivalens. Beslut, hvad spørgsmålet stiller – om det er koncentrationen af analytten, pH-værdien på et bestemt trin eller pH-værdien ved ækvivalens.
Trin 4:Skriv den balancerede ligning
Skriv den støkiometriske ligning for syre-base reaktionen. Brug det til at bestemme molforholdet mellem reaktanter, som vil være nødvendigt, når mol omdannes til koncentration.
Trin 5:Beregn pH ved de ønskede punkter
Afhængigt af syre/base-styrkerne skal du bruge en af følgende fremgangsmåder:
- Stærk syre ↔ stærk base – pH =–log[syre]. Træk mol tilsat titrant fra, divider med det samlede volumen.
- Stærk base ↔ stærk syre – Følg de samme trin, men beregn først pOH:pOH =–log[base]. Konverter til pH med
pH = 14 – pOH. - Svag syre ↔ stærk base – Anvend Henderson-Hasselbalch-ligningen:
pH = pKₐ + log([A⁻]/[HA]). Koncentrationen af konjugatbasen er lig med antallet af tilsat mol titrant divideret med det samlede volumen. - Svag base ↔ stærk syre – Brug den konjugerede form:
pOH = pK_b + log([BH⁺]/[B]), og konverter derefter til pH.
For pKₐ-værdierne for almindelige svage syrer, se referencetabellen.
Trin 6:Find pH ved ækvivalens
• Stærk syre + stærk base – pH ≈7.
• Stærk syre + svag base – Beregn koncentrationen af konjugatbasen ved ækvivalens, tag –log for at opnå pOH, omregn derefter til pH.
• Stærk base + svag syre – Samme procedure, men start fra pOH og konverter til pH.
Trin 7:Bestem den oprindelige koncentration af analytten
Multiplicer mængden af tilsat titrant for at opnå ækvivalens med dens molaritet for at opnå mol titrant. Multiplicer med det støkiometriske forhold fra trin 4 for at finde mol analyt, der oprindeligt var til stede. Divider med det oprindelige analytvolumen for at få dens koncentration.
TL;DR
Antag en støkiometri på 1:1 for de fleste generelkemi-titreringer, og følg trinene ovenfor for at løse ethvert problem.
Advarsel
Inkluder altid mængden af tilsat titrant ved beregning af koncentrationer før eller ved ækvivalenspunktet.
Sidste artikelKalorimeterkonstant:Trin-for-trin kalibreringsvejledning
Næste artikelMestring af kemiske ligninger:En trin-for-trin guide
 Varme artikler
Varme artikler
-
 Enzym -actionfilm viser, hvordan naturen laver penicillinerKredit:CC0 Public Domain Forskere, der er specialiserede i at studere atom-for-atom-koreografi af enzymer, har afsløret ny indsigt i funktionen af isopenicillin N-syntase, et enzym, der er nødve
Enzym -actionfilm viser, hvordan naturen laver penicillinerKredit:CC0 Public Domain Forskere, der er specialiserede i at studere atom-for-atom-koreografi af enzymer, har afsløret ny indsigt i funktionen af isopenicillin N-syntase, et enzym, der er nødve -
 Origami inspirerer til ny teknologi til vævsregenereringUMass Lowell Prof. Gulden Camci-Unal arbejder sammen med studerende Xinchen Wu om biomaterialeforskning ved universitetets Saab Emerging Technologies and Innovation Center. Kredit:Edwin Aguirre for UM
Origami inspirerer til ny teknologi til vævsregenereringUMass Lowell Prof. Gulden Camci-Unal arbejder sammen med studerende Xinchen Wu om biomaterialeforskning ved universitetets Saab Emerging Technologies and Innovation Center. Kredit:Edwin Aguirre for UM -
 Direkte metanomdannelse under milde forhold ved termo-, elektro- eller fotokatalyse gennemgåetMethans molekylære struktur (til venstre) og skematisk illustration af et energidiagram for lavtemperatur-metanaktivering i elektro- og fotoaktiveringsinvolverede reaktionssystemer (højre). Kredit:MEN
Direkte metanomdannelse under milde forhold ved termo-, elektro- eller fotokatalyse gennemgåetMethans molekylære struktur (til venstre) og skematisk illustration af et energidiagram for lavtemperatur-metanaktivering i elektro- og fotoaktiveringsinvolverede reaktionssystemer (højre). Kredit:MEN -
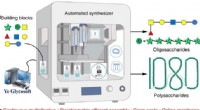 Automatisk kulhydratsynthesizer producerer polysaccharider af rekordlængdeGrafisk abstrakt. Kredit:Nature Synthesis (2022). DOI:10.1038/s44160-022-00171-9 Et team af forskere med medlemmer fra Peking University og WuXi AppTec (Tianjin) Co., Ltd., har designet og bygget e
Automatisk kulhydratsynthesizer producerer polysaccharider af rekordlængdeGrafisk abstrakt. Kredit:Nature Synthesis (2022). DOI:10.1038/s44160-022-00171-9 Et team af forskere med medlemmer fra Peking University og WuXi AppTec (Tianjin) Co., Ltd., har designet og bygget e


