Metaller og saltsyre:Reaktivitet og reaktioner
Metaller, der reagerer med HCl for at producere hydrogengas (H₂):
* Gruppe 1 (alkalimetaller): Lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cæsium (Cs), Francium (Fr) - Disse metaller reagerer kraftigt, nogle gange eksplosivt.
* Gruppe 2 (jordalkalimetaller): Beryllium (Be), Magnesium (Mg), Calcium (Ca), Strontium (Sr), Barium (Ba), Radium (Ra) - Reaktiviteten stiger ned i gruppen.
* Aluminium (Al): Reagerer langsomt ved stuetemperatur, men hurtigere ved opvarmning.
* Zink (Zn): Reagerer let.
* Jern (Fe): Reagerer langsomt ved stuetemperatur, hurtigere med varme.
* Tin (Sn): Reagerer langsomt.
* Mangan (Mn): Reagerer let.
Metaller, der IKKE reagerer med HCl:
* Kobber (Cu):
* Sølv (Ag):
* Guld (Au):
* Platin (Pt):
Forklaring:
Reaktiviteten af metaller med syrer er relateret til deres position i den elektrokemiske serie. Metaller højere i serien er mere reaktive og vil fortrænge brint fra syrer.
Nøglepunkter:
* Danning af hydrogengas: Reaktionen mellem et metal og HCl producerer typisk hydrogengas (H2) som et biprodukt. Det er derfor, man ofte ser, at der dannes bobler, når et metal reagerer med HCl.
* Metalhalogenidsalt: Metallet danner også et metalhalogenidsalt. For eksempel reagerer zink med HCl og danner zinkchlorid (ZnCl2) og hydrogengas.
* Undtagelser: Der er nogle undtagelser fra disse generelle regler. For eksempel danner nogle metaller som aluminium et beskyttende oxidlag, der kan forhindre yderligere reaktion med HCl.
Lad mig vide, hvis du vil have flere detaljer om et bestemt metal!
Sidste artikelNatriumhydroxid i vand:opløsning vs. suspension forklaret
Næste artikelAlkymiens syv metaller:egenskaber og symbolisme
 Varme artikler
Varme artikler
-
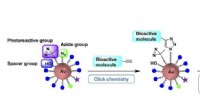 Let monterede guld nanopartikel stilladser tjener som molekylær sondeEt-trins forberedelse af fotoaffinitetsprober ved hjælp af klikbare guld-nanopartikel-prækursorer muliggør hensigtsmæssige målidentifikationsundersøgelser Kredit:Figur modificeret fra organisk og biom
Let monterede guld nanopartikel stilladser tjener som molekylær sondeEt-trins forberedelse af fotoaffinitetsprober ved hjælp af klikbare guld-nanopartikel-prækursorer muliggør hensigtsmæssige målidentifikationsundersøgelser Kredit:Figur modificeret fra organisk og biom -
 Forfalsket arganolie afdækket gennem ny analysemetodeKredit:CC0 Public Domain Forskere fra Quadram Institute har udviklet en ny måde at teste ægtheden af arganolie på, en af verdens dyreste spiseolier. I de seneste år, det er blevet eftertragtet
Forfalsket arganolie afdækket gennem ny analysemetodeKredit:CC0 Public Domain Forskere fra Quadram Institute har udviklet en ny måde at teste ægtheden af arganolie på, en af verdens dyreste spiseolier. I de seneste år, det er blevet eftertragtet -
 Hvordan temperatur påvirker isbjergsmeltning:en ekspertoversigtDC Productions/Photodisc/Getty Images Forstå isbjergets smeltning Isbjerge, de kolossale flydende masser af ferskvandsis, der driver hen over verdenshavene, er formet af temperaturen på vandet, der o
Hvordan temperatur påvirker isbjergsmeltning:en ekspertoversigtDC Productions/Photodisc/Getty Images Forstå isbjergets smeltning Isbjerge, de kolossale flydende masser af ferskvandsis, der driver hen over verdenshavene, er formet af temperaturen på vandet, der o -
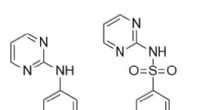 Et antibiotikum, der forklæder sig som en naturlig forbindelse i den gigantiske Madeira-svinDen kemiske forbindelse, som forskerne troede, de opdagede (til venstre) - og hvad de virkelig havde fundet (til højre). Kredit:Luke Robertson En tidligere undersøgelse har vist, at en type fjel,
Et antibiotikum, der forklæder sig som en naturlig forbindelse i den gigantiske Madeira-svinDen kemiske forbindelse, som forskerne troede, de opdagede (til venstre) - og hvad de virkelig havde fundet (til højre). Kredit:Luke Robertson En tidligere undersøgelse har vist, at en type fjel,
- Hvilken energi opbevares i midten af atomer?
- Group udvikler teknik til at forme pulser af intens infrarødt lys
- Hvordan genereres elektricitet fra rindende vand?
- Hvilken type hvide blodlegemer spiller en vigtig rolle i immunitet mod infektionssygdomme?
- Ny udvikling med kinesiske satellitter i løbet af det sidste årti
- Hvad er egenskaber ved fysisk ejendom?


