Lewis-struktur og ikke-bindende elektroner til CH2Br2 (dibrommethan)
1. Bestem det samlede antal valenselektroner:
* Kulstof (C) har 4 valenselektroner.
* Brint (H) har 1 valenselektron hver (2 i alt).
* Brom (Br) har 7 valenselektroner hver (14 i alt).
Samlede valenselektroner =4 + 2 + 14 =20
2. Bestem det centrale atom:
* Kulstof er det mindst elektronegative atom, så det vil være det centrale atom.
3. Tegn en enkelt binding mellem det centrale atom og de omgivende atomer:
* Forbind carbonatomet til de to brintatomer og de to bromatomer med enkeltbindinger.
4. Fuldfør oktetterne af de omgivende atomer:
* Hvert brintatom har brug for 2 elektroner for at fuldføre sin duet.
* Hvert bromatom har brug for 8 elektroner for at fuldføre sin oktet.
5. Fuldfør oktetten af det centrale atom (hvis nødvendigt):
* Kulstof har 4 elektroner fra enkeltbindingerne. Den har brug for 4 elektroner mere for at fuldføre sin oktet.
6. Tilføj ensomme par til de omgivende atomer:
* Hvert bromatom har 3 ensomme par (6 elektroner) for at fuldende sin oktet.
Lewis-struktur:
```
H
|
H - C - Br
|
Br
```
Ikke-bindende elektroner:
* Hvert bromatom har 6 ikke-bindende elektroner (3 ensomme par).
* Der er to bromatomer, så der er i alt 12 ikke-bindende elektroner.
Derfor er der 12 ikke-bindende elektroner i CH2Br2.
 Varme artikler
Varme artikler
-
 Sådan laver du spiseligt slim:13 sikre, sjove opskrifter til børnPhotoLife_Style/Shutterstock Slime tilbyder en engagerende sanseoplevelse, der glæder både børn og voksne. Mens de fleste husholdningsopskrifter er afhængige af borax, lim eller andre kemikalier, der
Sådan laver du spiseligt slim:13 sikre, sjove opskrifter til børnPhotoLife_Style/Shutterstock Slime tilbyder en engagerende sanseoplevelse, der glæder både børn og voksne. Mens de fleste husholdningsopskrifter er afhængige af borax, lim eller andre kemikalier, der -
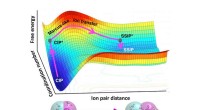 Elegant teori viser, hvordan vand hjælper med at adskille ioner involveret i materialesyntese og -f…Adskillelsen (bunden) af lithiumfluorid (Li og F) ionpar involverer to trin:(1) en forøgelse af vandkoordinationen omkring ionerne (kontaktionpar, CIP til CIP*) og (2) rumlig adskillelse af ionerne (C
Elegant teori viser, hvordan vand hjælper med at adskille ioner involveret i materialesyntese og -f…Adskillelsen (bunden) af lithiumfluorid (Li og F) ionpar involverer to trin:(1) en forøgelse af vandkoordinationen omkring ionerne (kontaktionpar, CIP til CIP*) og (2) rumlig adskillelse af ionerne (C -
 Forskere afslører mekanisme for dioxygenaktiveringKredit:Pixabay/CC0 Public Domain Metalloenzym kan koble dioxygenaktivering til substratfunktionalisering, som ofte udviser uovertruffen effektivitet, selv under omgivende forhold. Det menes, at m
Forskere afslører mekanisme for dioxygenaktiveringKredit:Pixabay/CC0 Public Domain Metalloenzym kan koble dioxygenaktivering til substratfunktionalisering, som ofte udviser uovertruffen effektivitet, selv under omgivende forhold. Det menes, at m -
 Forskere opnåede nye forbindelser med potentiel antitumoreffekt fra havsvampDen store del af forskningen relateret til syntese af målforbindelser blev udført af Polina Smirnova - en ph.d. studerende ved Institut for organisk kemi i SNS FEFU. Kredit:FEFUs pressekontor Kemi
Forskere opnåede nye forbindelser med potentiel antitumoreffekt fra havsvampDen store del af forskningen relateret til syntese af målforbindelser blev udført af Polina Smirnova - en ph.d. studerende ved Institut for organisk kemi i SNS FEFU. Kredit:FEFUs pressekontor Kemi
- Tryk giver den bedste afkøling
- En alfa-partikelopladning 2,0e sendes i høj hastighed mod en guldkerne 79E Hvad den elektriske kraf…
- Rumvandrende astronauter tjekker stedet for kapsellækage
- Hvordan kommer DDT ind i kroppen af zooplankton?
- Effektiv kuldioxidreduktion under synligt lys med en ny, billig katalysator
- Hvilken type væske rustes metal hurtigst i?


