Frysningsprocessen:Forstå overgangen fra væske til fast stof
* Reduceret kinetisk energi: Molekylerne i en væske bevæger sig konstant og kolliderer med hinanden. Når væsken afkøles, falder dens temperatur, hvilket betyder, at molekylerne har mindre kinetisk energi. Dette får dem til at bremse.
* Reduceret mellemrum: Efterhånden som molekylerne sænker farten, mister de evnen til at overvinde tiltrækningskræfterne mellem dem. Dette får molekylerne til at bevæge sig tættere sammen, hvilket mindsker afstanden mellem dem.
* Danning af et almindeligt gitter: Med den reducerede afstand og langsommere bevægelse bliver molekylerne mere organiserede og arrangerer sig selv i et fast, gentaget mønster kaldet et krystalgitter. Dette giver det faste stof sin stive struktur.
* Ændring i tilstand: Når molekylerne er låst fast i krystalgitteret, er stoffet gået fra en væske til et fast stof. Dette er karakteriseret ved et fast volumen og form.
Vigtigste ting at huske ved frysning:
* Temperaturen forbliver konstant: Under frysning forbliver stoffets temperatur konstant, selvom varme fjernes. Dette skyldes, at varmeenergien bliver brugt til at bryde bindingerne mellem molekyler i flydende tilstand.
* Frysepunkt: Hvert stof har et bestemt frysepunkt, hvor det går fra flydende til fast stof. Dette punkt bestemmes af styrken af de intermolekylære kræfter mellem molekylerne.
Eksempler på frysning:
* Vand fryser til is
* Smeltet lava størkner til sten
* Flydende kviksølv bliver til fast kviksølv
Fortæl mig, hvis du gerne vil dykke dybere ned i videnskaben bag frysning, eller har nogle specifikke spørgsmål!
Sidste artikelFluor vs. Brom Atomradius:Hvilken er større?
Næste artikelAlmindelige kemiske indikatorer:væske- og papirtyper og anvendelser
 Varme artikler
Varme artikler
-
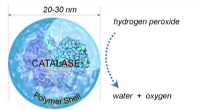 Fælles antioxidantenzym kan give potentiel behandling for COVID-19Simpelt diagram, der viser katalase kickstartreaktion, der omdanner hydrogenperoxid til vand og oxygen. Kredit:Yunfeng Lu forskningsgruppe/UCLA Forskere fra UCLA og Kina har fundet ud af, at katal
Fælles antioxidantenzym kan give potentiel behandling for COVID-19Simpelt diagram, der viser katalase kickstartreaktion, der omdanner hydrogenperoxid til vand og oxygen. Kredit:Yunfeng Lu forskningsgruppe/UCLA Forskere fra UCLA og Kina har fundet ud af, at katal -
 Transformering af kuldioxid – forskere udvikler ny to-trins CO2-konverteringsteknologiUD Professor Feng Jiaos team konstruerede en elektrolysator, afbilledet her, at gennemføre deres nye to-trins konverteringsproces. Kredit:Feng Jiao Et team af forskere ved University of Delawares
Transformering af kuldioxid – forskere udvikler ny to-trins CO2-konverteringsteknologiUD Professor Feng Jiaos team konstruerede en elektrolysator, afbilledet her, at gennemføre deres nye to-trins konverteringsproces. Kredit:Feng Jiao Et team af forskere ved University of Delawares -
 Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummetDette sammensatte billede viser en illustration af en kulstofrig rød kæmpestjerne (midten), der opvarmer en exoplanet (nederst til venstre) og en overlejring af en nyfundet vej, der kunne gøre det mul
Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummetDette sammensatte billede viser en illustration af en kulstofrig rød kæmpestjerne (midten), der opvarmer en exoplanet (nederst til venstre) og en overlejring af en nyfundet vej, der kunne gøre det mul -
 Ny, fuldt bionedbrydelig cellulosemembran viser sig effektiv til olie-vand-separationDen lukkede kredsløbsproces af den nedbrydelige celluloseolie-vand-separationsmembran. Kredit:Institute of Coal Chemistry (CAS) Olieudslip og industriel forurening udgør en enorm trussel mod det øk
Ny, fuldt bionedbrydelig cellulosemembran viser sig effektiv til olie-vand-separationDen lukkede kredsløbsproces af den nedbrydelige celluloseolie-vand-separationsmembran. Kredit:Institute of Coal Chemistry (CAS) Olieudslip og industriel forurening udgør en enorm trussel mod det øk
- Marcus regime i organiske enheder - grænsefladeladningsoverførselsmekanisme verificeret
- Ny probe for stofskiftesygdomme
- Antarktiske sæler kan hjælpe med at forudsige isdelssmeltning
- Hvilken slags energi bruger vandmølle?
- Har superstation om kometer og asteroider videnskabeligt grundlag?
- Forskere blander det ublandbare for at skabe chokerende nanopartikler


