Beregning af oxidationstal:En trin-for-trin guide til H2C2O4, Mn2O7, Hg2Cl2 og IF5
1. H2C2O4 (Oxalsyre)
* H: Brint har normalt et oxidationstal på +1. Da der er to brintatomer, er det samlede bidrag fra brint +2.
* O: Ilt har typisk et oxidationstal på -2. Med fire iltatomer er det samlede bidrag fra ilt -8.
* C: Lad oxidationstallet for kulstof være 'x'. Der er to kulstofatomer, så deres samlede bidrag er 2x.
For at finde 'x' kan vi bruge det faktum, at summen af oxidationstallene i en neutral forbindelse er nul:
+2 + 2x - 8 =0
2x =+6
x =+3
Derfor er oxidationstallene:
* H:+1
* C:+3
* O:-2
2. Mn207 (mangan(VII)oxid)
* O: Ilt har et oxidationstal på -2, og der er syv oxygenatomer, i alt -14.
* Mn: Lad oxidationstallet for mangan være 'y'. Da der er to manganatomer, er det samlede bidrag 2y.
Summen af oxidationstallene er nul:
2y - 14 =0
2y =+14
y =+7
Derfor er oxidationstallene:
* Mn:+7
* O:-2
3. Hg2Cl2 (kviksølv(I)chlorid)
* Cl: Klor har normalt et oxidationstal på -1. Der er to kloratomer, der i alt bidrager med -2.
* Hg: Lad oxidationstallet for kviksølv være 'z'. Da der er to kviksølvatomer, er det samlede bidrag 2z.
Summen af oxidationstallene er nul:
2z - 2 =0
2z =+2
z =+1
Derfor er oxidationstallene:
* Hg:+1
* Cl:-1
4. IF₅ (jodpentafluorid)
* F: Fluor har altid et oxidationstal på -1. Der er fem fluoratomer, der i alt bidrager med -5.
* Jeg: Lad oxidationstallet for jod være 'w'.
Summen af oxidationstallene er nul:
w - 5 =0
w =+5
Derfor er oxidationstallene:
* Jeg:+5
* F:-1
Sidste artikelRødt farvestof:naturlige vs. syntetiske kilder og hvad de er lavet af
Næste artikelFordele ved faste, flydende og gastilstande
 Varme artikler
Varme artikler
-
 Forskere kan regne med forbedret proteomikmetodePrinceton Universitys Martin Wühr har forbedret sin metode til nøjagtigt at tælle de proteiner, der er til stede i en celle under forskellige omstændigheder. TMc+-metoden er i en slags sweet spot samm
Forskere kan regne med forbedret proteomikmetodePrinceton Universitys Martin Wühr har forbedret sin metode til nøjagtigt at tælle de proteiner, der er til stede i en celle under forskellige omstændigheder. TMc+-metoden er i en slags sweet spot samm -
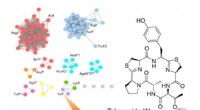 Genomminedrift fører til en ny type peptidprenyleringFigur 1:Målrettet genom -minedrift af prenyltransferaser identificerede TolF -enzymet og tol biosyntetisk genklynge (BGC). Øverst til venstre viser et proteinsekvens -lighednetværk af prenyltransfer
Genomminedrift fører til en ny type peptidprenyleringFigur 1:Målrettet genom -minedrift af prenyltransferaser identificerede TolF -enzymet og tol biosyntetisk genklynge (BGC). Øverst til venstre viser et proteinsekvens -lighednetværk af prenyltransfer -
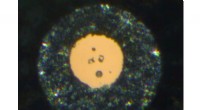 Højtryk skaber nye naboer til berylliumHurlbutitkrystaller (i midten) i diamantamboltcellen, der blev brugt til højtryksforsøgene. Krystallerne er hver omkring 0,01 millimeter store. Kredit:DESY, Anna Pakhomova Det sjældne grundstof be
Højtryk skaber nye naboer til berylliumHurlbutitkrystaller (i midten) i diamantamboltcellen, der blev brugt til højtryksforsøgene. Krystallerne er hver omkring 0,01 millimeter store. Kredit:DESY, Anna Pakhomova Det sjældne grundstof be -
 Duften af gamle bøger kunne hjælpe med at bevare demEn fiber placeres mellem siderne i en gammel bog for at samle lugte. Kredit:Tilpasset fra ACS -sensorer 2019, Gamle bøger afgiver en kompleks blanding af lugte, lige fra behagelige (mandler, kar
Duften af gamle bøger kunne hjælpe med at bevare demEn fiber placeres mellem siderne i en gammel bog for at samle lugte. Kredit:Tilpasset fra ACS -sensorer 2019, Gamle bøger afgiver en kompleks blanding af lugte, lige fra behagelige (mandler, kar
- Har Facebook-data hjulpet Trump? Great Hack udforsker skandale
- Forskere demonstrerer en metode, der reducerer friktionen mellem to overflader til næsten nul i mak…
- Navnet på Tooley-krateret
- Hvad er identifikationstesten for brintgas?
- Drevet af kunstig intelligens sporer teknologi fugleaktivitet på solanlæg
- Jordbundsundersøgelse viser, at Australien er mest afklædt


