Genomminedrift fører til en ny type peptidprenylering
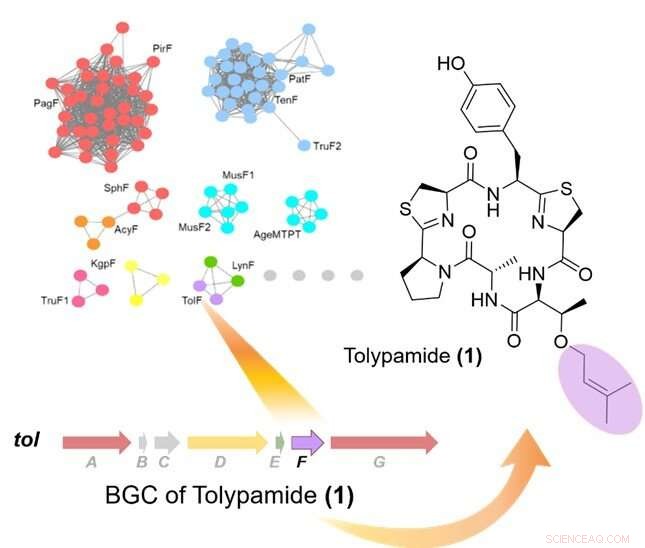
Figur 1:Målrettet genom -minedrift af prenyltransferaser identificerede TolF -enzymet og tol biosyntetisk genklynge (BGC). Øverst til venstre viser et proteinsekvens -lighednetværk af prenyltransferaser. Den biosyntetiske genklynge for tol pathway er vist og var forbundet med biosyntesen af tolypamid. Tolypamid indeholder en fremadrettet prenyleret threoninrest (farvet i lilla). Kredit:National University of Singapore
Forskere fra NUS brugte en genomminedrift til at identificere et nyt cyklisk peptid (tolypamid) afledt af et cyanobakterium. Biosyntesen af tolypamid indeholder en ny type enzym, der er i stand til at prænylere en række substrater og har potentiel brug i farmaceutisk kemi og syntetisk biologi.
Bioaktive peptider har sikret sig en højborg på det farmaceutiske marked på grund af de mange fordele, såsom effektiv målretning af protein-protein-interaktioner, lave effekter uden for målet, og lav toksicitet. Disse fordele kompromitteres ofte på grund af dårlig biotilgængelighed og cellepermeabilitet. En måde at forbedre membranpermeabiliteten på er at øge lipofiliteten ved at tilføje en alkylkæde til molekylet (prenylering). Disse transformationer, som kan katalyseres af enzymer involveret i biosyntesen af cyanobactin naturlige produkter, kan potentielt øge den terapeutiske effekt af umodificerede peptider. Også, cyanobactin-enzymer har bred substratselektivitet og virker på en meget selektiv og specifik måde med hensyn til positionen og orienteringen af aminosyreresterne. At forstå begrundelsen bag selektiviteten og specificiteten af disse katalysatorer vil hjælpe med at udnytte disse enzymers evne som biokemiske værktøjssæt.
I samarbejde med et internationalt forskerhold, Prof Brandon Morinaka fra Institut for Farmaci, National University of Singapore opdagede en ny type cyanobactin-enzym kendt som ToIF. Det udviser specifik selektivitet til modifikation af serin- og threoninrester i peptider. Dette arbejde er en fælles forskningsindsats med prof. Eric Schmidt fra University of Utah og Dr. Muriel Gugger fra Institut Pasteur. Proteiner fra en underfamilie af prenyltransferaser blev kortlagt til et sekvenslignende netværk.
Forskerne anvendte målrettet minedrift til at analysere genklyngerne, der koder for disse proteiner, og identificerede ToIF -enzym og tol biosyntetisk vej. De fandt ud af, at TolF -enzymet er involveret i produktionen af tolypamid, som har en hydrofob prenylfunktionel gruppe knyttet til dets struktur (figur 1). Sådanne molekylære vedhæftninger er nyttige til forbedring af membranpermeabiliteten af terapeutiske forbindelser. TolF -enzymet blev funktionelt valideret ved in vitro biosyntese af tolypamid -naturproduktet (figur 2). Yderligere biokemiske assays viser, at TolF -enzymet også er i stand til at lette fremadgående prenylering af threonin- og serinresterne på forskellige syntetiske peptider.
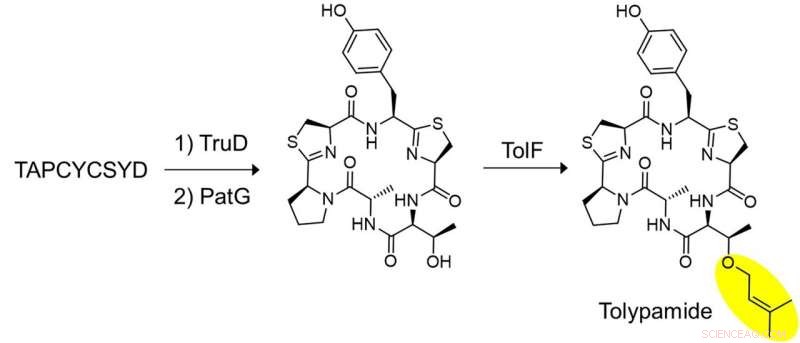
Figur 2:In vitro biosyntese af tolypamid og funktionel validering af TolF. Et centralt sæt eksperimenter blev udført for at vise, at TolF virker på det heterocykliserede cykliske peptid. Det syntetiserede peptid, TAPCYCSYD blev inkuberet sekventielt med enzymerne, TruD (heterocyclase) og PatG (makrocyclase) for at tilvejebringe det heterocykliserede cykliske peptid. Inkubation med TolF gav kvantitativ omdannelse til det naturlige produkt tolypamid. Kredit:National University of Singapore
Til dato, det eneste andet medlem af denne klasse af enzymer (prenyltransferase), der er identificeret til at virke på serin- eller threoninrester, er TruF1. Imidlertid, dets dårlige opløselighed og lave in vitro -aktivitet har forhindret omfattende karakterisering. Opdagelsen af TolF giver mulighed for at studere strukturbiologien og udviklingen af denne enzymfamilie.
Prof Morinaka sagde, "Yderligere karakterisering af TolF-enzymet vil muliggøre en mere fuldstændig forståelse af substratspecificitet og selektivitet af prenyltransferaser. Dette vil lette den rationelle konstruktion af disse biokatalysatorer som kraftfulde værktøjer inden for syntetisk biologi."
 Varme artikler
Varme artikler
-
 Vedvarende opløsningsmidler afledt af lignin sænker spild i biobrændstofproduktionBioraffinaderi-konceptet, der bruger fornybare dybe eutektiske opløsningsmidler (DES) afledt af ligninråvarer, er vist her. Kredit:US Department of Energy Et bioraffinaderi med lukket kredsløb kan
Vedvarende opløsningsmidler afledt af lignin sænker spild i biobrændstofproduktionBioraffinaderi-konceptet, der bruger fornybare dybe eutektiske opløsningsmidler (DES) afledt af ligninråvarer, er vist her. Kredit:US Department of Energy Et bioraffinaderi med lukket kredsløb kan -
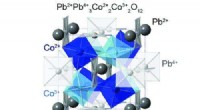 Blandede valenstilstande i blyperovskitterKrystalstruktur af Pb2+Pb4+3Co2+2Co3+2O12, hvor Pb og Co har ladningsordener på trods af den simple PbCoO3-kemiske sammensætning og valensfordelingsændringer for PbMO3 (M:3d overgangsmetal). Kredit: J
Blandede valenstilstande i blyperovskitterKrystalstruktur af Pb2+Pb4+3Co2+2Co3+2O12, hvor Pb og Co har ladningsordener på trods af den simple PbCoO3-kemiske sammensætning og valensfordelingsændringer for PbMO3 (M:3d overgangsmetal). Kredit: J -
 MOF-baseret sensor til test af vandkvalitetBegreber brugt i tech-demo-designet:Identifikation af vandkvalitetsproblemet i den lokale befolkning, ændring af bomuld for at udsende lys, der angiver fluoridindholdet, tech-demo design og konstrukti
MOF-baseret sensor til test af vandkvalitetBegreber brugt i tech-demo-designet:Identifikation af vandkvalitetsproblemet i den lokale befolkning, ændring af bomuld for at udsende lys, der angiver fluoridindholdet, tech-demo design og konstrukti -
 Video:Hvordan kommunikerer planter med hinanden?Kredit:The American Chemical Society Forår er i luften! Det er tid til at slå græsplænen og indånde duften af nyslået græs. Men denne behagelige forårsduft kan faktisk være et kemisk råb om hjæ
Video:Hvordan kommunikerer planter med hinanden?Kredit:The American Chemical Society Forår er i luften! Det er tid til at slå græsplænen og indånde duften af nyslået græs. Men denne behagelige forårsduft kan faktisk være et kemisk råb om hjæ
- Tryk tilbage:Sony Walkman udløser nostalgi på 40 års fødselsdag
- NASAs TROPICS Pathfinder-satellit producerer globale første lysbilleder og fanger orkanen Ida
- Indstillelige elektroniske egenskaber til metallofullerener
- S, N co-doteret carbon nanorør-indkapslet CoS2@Co
- Sådan fungerer Planet Hunting
- Sådan beregnes diameter kun med længde og bredde


