Ioniske bindinger:Forståelse af elektrostatisk tiltrækning mellem atomer
Her er en opdeling:
* Elektrostatisk tiltrækning: Dette refererer til tiltrækningskraften mellem modsat ladede objekter.
* Atomer med modsatte ladninger: I en ionbinding mister det ene atom (metallet) elektroner og bliver positivt ladet (kation), mens det andet atom (ikke-metallet) får elektroner og bliver negativt ladet (anion).
Nøglekarakteristika for ioniske bindinger:
* Stærke bånd: Ionbindinger er generelt stærke på grund af den stærke elektrostatiske tiltrækning mellem ionerne.
* Høje smelte- og kogepunkter: Styrken af bindingerne betyder, at ioniske forbindelser typisk har høje smelte- og kogepunkter.
* Fast ved stuetemperatur: De fleste ioniske forbindelser er faste ved stuetemperatur.
* Leder elektricitet i flydende eller vandige opløsninger: Når de er opløst eller smeltet, bliver ionerne frie til at bevæge sig, hvilket giver dem mulighed for at lede elektricitet.
Eksempel:
Natriumchlorid (NaCl) er et klassisk eksempel på en ionforbindelse. Natrium (Na) mister en elektron for at blive en positivt ladet natriumion (Na+), og klor (Cl) får en elektron til at blive en negativt ladet chloridion (Cl-). Den elektrostatiske tiltrækning mellem disse modsat ladede ioner danner den ioniske binding, der holder forbindelsen sammen.
 Varme artikler
Varme artikler
-
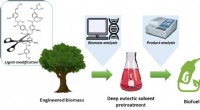 Team udvikler biobrændstofproduktionsproces i samarbejde med nordamerikanske forskereForskerne var i stand til at maksimere og kombinere potentialet i flere forskellige områder for produktion af biobrændstoffer, herunder genteknologi, procesteknologi, og analyseteknologi. Kredit:Korea
Team udvikler biobrændstofproduktionsproces i samarbejde med nordamerikanske forskereForskerne var i stand til at maksimere og kombinere potentialet i flere forskellige områder for produktion af biobrændstoffer, herunder genteknologi, procesteknologi, og analyseteknologi. Kredit:Korea -
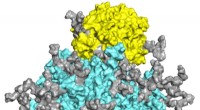 Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit
Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit -
 Det er ikke vibranium eller proto-adamantium, men forskeres nye legering kommer tæt påKredit:University of North Texas Fire gange stærkere end rustfrit stål, en unik legering blander krom, kobolt, jern, mangan og silicium. Det er ikke Black Panthers vibranium eller Captain America
Det er ikke vibranium eller proto-adamantium, men forskeres nye legering kommer tæt påKredit:University of North Texas Fire gange stærkere end rustfrit stål, en unik legering blander krom, kobolt, jern, mangan og silicium. Det er ikke Black Panthers vibranium eller Captain America -
 Video:Nobelprisen i kemi 2017:Cryo-elektronmikroskopi forklaretKredit:The American Chemical Society Jacques Dubochet, Joachim Frank og Richard Henderson har krævet årets Nobelpris i kemi. Trioen tjente prisen for deres arbejde med kryo-elektronmikroskopi, so
Video:Nobelprisen i kemi 2017:Cryo-elektronmikroskopi forklaretKredit:The American Chemical Society Jacques Dubochet, Joachim Frank og Richard Henderson har krævet årets Nobelpris i kemi. Trioen tjente prisen for deres arbejde med kryo-elektronmikroskopi, so


