Forståelse af tryk i butancylindre:et molekylært perspektiv
1. Gassernes natur
* Kinetisk molekylær teori: Gasser er opbygget af bittesmå molekyler, der er i konstant tilfældig bevægelse. Denne bevægelse er det, vi kalder kinetisk energi.
* Kollisioner: Disse molekyler kolliderer konstant med hinanden og væggene i deres beholder.
2. Tryk forklaret
* Kraft pr. område: Tryk er defineret som den kraft, der udøves pr. arealenhed.
* Kollisioner og kraft: Når butanmolekyler kolliderer med cylinderens indvendige vægge, udøver de en lille kraft på overfladen. Jo flere kollisioner der er, jo større kraft.
* Tryk opbygges: Fordi disse kollisioner sker konstant, skaber de en kontinuerlig kraft på cylinderens vægge. Denne vedvarende kraft resulterer i det tryk, vi måler inde i cylinderen.
3. Faktorer, der påvirker tryk
* Temperatur: Højere temperatur betyder hurtigere bevægelige molekyler, hvilket fører til hyppigere og kraftigere kollisioner, hvilket resulterer i højere tryk.
* Lydstyrke: Formindskelse af cylinderens volumen (komprimering af gassen) betyder, at molekylerne har mindre plads og kolliderer oftere, hvilket fører til højere tryk.
* Antal molekyler: Flere molekyler i cylinderen betyder flere kollisioner og højere tryk.
4. Butan i cylinderen
* Flydende gas: Butan opbevares i cylinderen som en flydende gas under tryk.
* Damptryk: Selvom butanen hovedsageligt er en væske, er der altid noget butandamp over væsken. Denne damp udøver tryk på cylindervæggene.
* Ligevægt: Trykket i cylinderen bestemmes af ligevægten mellem væske- og dampfasen af butanen. Trykket vil stige, når temperaturen stiger, hvilket får mere butan til at fordampe.
Opsummering: Trykket inde i en butancylinder er et direkte resultat af det konstante bombardement af cylindervæggene af hurtigt bevægende butanmolekyler. Frekvensen og kraften af disse kollisioner bestemmer trykket, som påvirkes af temperatur, volumen og mængden af tilstedeværende butan.
 Varme artikler
Varme artikler
-
 Kræft målrettet med genanvendelig brændenældebehandlingRepræsentation af den organiske osmiumforbindelse, som udløses ved hjælp af en ikke-toksisk dosis natriumformiat, et naturligt produkt, der findes i mange organismer, herunder brændenælder og myrer. K
Kræft målrettet med genanvendelig brændenældebehandlingRepræsentation af den organiske osmiumforbindelse, som udløses ved hjælp af en ikke-toksisk dosis natriumformiat, et naturligt produkt, der findes i mange organismer, herunder brændenælder og myrer. K -
 Forskning peger på stærk indvirkning fra vandrensning til lægemiddelproduktionKredit:Pixabay/CC0 Public Domain Vand er underligt - og alligevel så vigtigt. Faktisk, det er et af de mest usædvanlige molekyler på Jorden. Det koger ved en temperatur det ikke burde. Det udvider
Forskning peger på stærk indvirkning fra vandrensning til lægemiddelproduktionKredit:Pixabay/CC0 Public Domain Vand er underligt - og alligevel så vigtigt. Faktisk, det er et af de mest usædvanlige molekyler på Jorden. Det koger ved en temperatur det ikke burde. Det udvider -
 MOF holder luftfugtigheden i Goldilocks -zonenFigurtekst/kredit:Når den relative luftfugtighed stiger, MOF går fra tør (yderst til venstre) til fuldstændigt fyldt med vandmolekyler (yderst til højre); vandmolekyler vist med blåt. Kredit:American
MOF holder luftfugtigheden i Goldilocks -zonenFigurtekst/kredit:Når den relative luftfugtighed stiger, MOF går fra tør (yderst til venstre) til fuldstændigt fyldt med vandmolekyler (yderst til højre); vandmolekyler vist med blåt. Kredit:American -
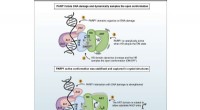 Forskere får ny indsigt i et dynamisk protein målrettet mod kræftbehandlingGrafisk abstrakt. Kredit:Élise Rouleau-Turcotte et al., Molecular Cell (2022). DOI:10.1016/j.molcel.2022.06.011 Ny strukturel information om et enzymmål i kræftmedicin kan hjælpe med udviklingen af
Forskere får ny indsigt i et dynamisk protein målrettet mod kræftbehandlingGrafisk abstrakt. Kredit:Élise Rouleau-Turcotte et al., Molecular Cell (2022). DOI:10.1016/j.molcel.2022.06.011 Ny strukturel information om et enzymmål i kræftmedicin kan hjælpe med udviklingen af
- Vælg nedenstående løsning, der ville producere en gennemsnitlig hastighed på nul?
- Er afstand størrelsen af hastigheden?
- Forskel mellem manipulerende og responderende variabel
- Æggene fra amfibier kan let tørre ud, fordi de?
- Robotforskere har pligt til at forhindre autonome våben
- Hvorfor var det vanskeligt for gamle græske forskere at definere energi?


