Atomstørrelse og ladning:Forståelse af atomstruktur
Her er en opdeling:
* Neutralt atom: I et neutralt atom er antallet af protoner (positiv ladning) lig med antallet af elektroner (negativ ladning). Elektronerne er fordelt i energiniveauer (skaller) rundt om kernen. Den yderste skal bestemmer atomets størrelse.
* Kationer (positivt ladede): Når et atom mister en elektron, bliver det til en kation. Dette tab af en elektron reducerer elektron-elektron frastødningen, hvilket fører til en mindre atomradius. Den yderste skal er nu tættere på kernen, da der er færre elektroner, der skærmer den.
* Anioner (negativt ladede): Når et atom får en elektron, bliver det til en anion. Den tilføjede elektron øger elektron-elektron frastødningen, hvilket fører til en større atomradius. Den yderste skal er nu længere fra kernen på grund af den øgede elektron-elektron frastødning.
Derfor er et atoms størrelse primært påvirket af antallet af elektronskaller og den effektive kerneladning, som de yderste elektroner oplever.
Nøglepunkter:
* Kationer er generelt mindre end deres neutrale atom-modstykker.
* Anioner er generelt større end deres neutrale atom-modstykker.
* Størrelsen af et atom er ikke udelukkende bestemt af dets ladning.
Eksempel:
* Natrium (Na) atom har en større radius end natriumion (Na+).
* Klor (Cl) atom har en mindre radius end chlor ion (Cl-).
Sammenfattende, selvom det er rigtigt, at kationer generelt er mindre end deres neutrale atom-modstykker, og anioner er større, er størrelsen af et atom et komplekst samspil af faktorer.
 Varme artikler
Varme artikler
-
 Dens regnende diamanter over hele universet, tyder forskning påUranus og Neptun, isgiganter, hvor videnskabsmænd mener, at diamantregn falder under overfladen. Det kan regne med diamanter på planeter i hele universet, foreslog videnskabsmænd fredag, efter at h
Dens regnende diamanter over hele universet, tyder forskning påUranus og Neptun, isgiganter, hvor videnskabsmænd mener, at diamantregn falder under overfladen. Det kan regne med diamanter på planeter i hele universet, foreslog videnskabsmænd fredag, efter at h -
 Hjælper medikamentafgivende partikler med at presse gennem en sprøjteKredit:CC0 Public Domain Mikropartikler tilbyder en lovende måde at levere flere doser af et lægemiddel eller en vaccine på én gang, fordi de kan designes til at frigive deres nyttelast med bestem
Hjælper medikamentafgivende partikler med at presse gennem en sprøjteKredit:CC0 Public Domain Mikropartikler tilbyder en lovende måde at levere flere doser af et lægemiddel eller en vaccine på én gang, fordi de kan designes til at frigive deres nyttelast med bestem -
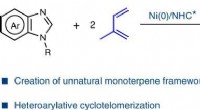 Forskere indser nikkel-katalyseret asymmetrisk heteroarylativ cyclotelomerisering af isoprenGrafisk abstrakt. Kredit:Nature Catalysis (2022). DOI:10.1038/s41929-022-00825-z Isopren bruges som en forløber til at producere terpener og terpenoider. Den direkte katalytiske omdannelse af isopr
Forskere indser nikkel-katalyseret asymmetrisk heteroarylativ cyclotelomerisering af isoprenGrafisk abstrakt. Kredit:Nature Catalysis (2022). DOI:10.1038/s41929-022-00825-z Isopren bruges som en forløber til at producere terpener og terpenoider. Den direkte katalytiske omdannelse af isopr -
 Strækbart, nedbrydelige halvledereEn ny strækbar halvleder, illustreret her, består af syrededbrydelige halvlederfibre (grønne) indlejret i en gummiagtig, bionedbrydeligt polymer. Kredit:Tilpasset fra ACS Central Science 2019, DOI:1
Strækbart, nedbrydelige halvledereEn ny strækbar halvleder, illustreret her, består af syrededbrydelige halvlederfibre (grønne) indlejret i en gummiagtig, bionedbrydeligt polymer. Kredit:Tilpasset fra ACS Central Science 2019, DOI:1
- Hvem var den første pige, der landede på månen?
- Hvor findes protease i din krop?
- Sammenligner vægten af mineraler med et lige volumenvand kaldet?
- Hvilke farver absorberer mere varme?
- United Airlines strammer livremmen, da virus rammer efterspørgslen
- Formlen for forbindelsen dannet mellem kalium og chloration er?


