Netto-ionligning:KClO4 + H2SO4 - Trin-for-trin-løsning
1. Skriv den afbalancerede molekylære ligning:
2KClO4 (aq) + H2SO4 (aq) → K2SO4 (aq) + 2HClO4 (aq)
2. Identificer de opløselige og uopløselige forbindelser:
Alle forbindelserne i denne reaktion er opløselige i vand.
3. Skriv hele den ioniske ligning:
2K⁺ (vandigt) + 2ClO4- (vandigt) + 2H⁺ (vandigt) + SO₄²⁻ (vandigt) → 2K⁺ (vandigt) + SO₄²⁻ (vandigt) + 2H+ (vandigt) + 2ClO₄q)⁻
4. Annuller tilskuerioner:
Bemærk, at kaliumionerne (K⁺) og perklorationer (ClO₄⁻) optræder på begge sider af ligningen. Disse er tilskuerioner, hvilket betyder, at de ikke deltager i selve reaktionen. Annuller dem.
5. Den nettoioniske ligning er:
2H+ (vandigt) + SO₄²⁻ (vandigt) → 2H+ (vandigt) + SO₄²⁻ (vandigt)
Vigtig bemærkning: Den nettoioniske ligning viser, at der ikke sker nogen egentlig reaktion mellem kaliumperchlorat og svovlsyre. Reaktanterne og produkterne er simpelthen opløste ioner i opløsning.
Sidste artikelOxidation:Forståelse af kemiske reaktioner med ilt
Næste artikelAtomstørrelse og ladning:Forståelse af atomstruktur
 Varme artikler
Varme artikler
-
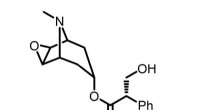 Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddelSwRI udvikler omkostningseffektive metoder til at syntetisere nye formuleringer til plantebaserede lægemidler, senest en syntetisk version af en populær behandling mod kvalme. Kredit:Southwest Researc
Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddelSwRI udvikler omkostningseffektive metoder til at syntetisere nye formuleringer til plantebaserede lægemidler, senest en syntetisk version af en populær behandling mod kvalme. Kredit:Southwest Researc -
 Genvinding af fosfor fra produktion af majsethanol kan hjælpe med at reducere grundvandsforureningVijay Singh, professor og direktør for Integrated Bioprocessing Research Lab, og Ankita Juneja, postdoktoral forskningsassistent i landbrugs- og biologisk teknik ved University of Illinois, viste, at
Genvinding af fosfor fra produktion af majsethanol kan hjælpe med at reducere grundvandsforureningVijay Singh, professor og direktør for Integrated Bioprocessing Research Lab, og Ankita Juneja, postdoktoral forskningsassistent i landbrugs- og biologisk teknik ved University of Illinois, viste, at -
 Molekylær spredning forbedrer kvasi-dobbeltlags organiske solcellerKredit:CC0 Public Domain I de sidste par år, organiske solceller (OSCer) baseret på ikke-fulleren (NF) acceptorer har vist enorme fremskridt med hensyn til effektkonverteringseffektivitet (PCE). S
Molekylær spredning forbedrer kvasi-dobbeltlags organiske solcellerKredit:CC0 Public Domain I de sidste par år, organiske solceller (OSCer) baseret på ikke-fulleren (NF) acceptorer har vist enorme fremskridt med hensyn til effektkonverteringseffektivitet (PCE). S -
 Forskere afkoder dynamikken i den største proteinnedbrydende maskine i atomare detaljerKredit:CC0 Public Domain Protein nanomaskiner lavet af flere proteinmolekyler er meget dynamiske under deres handlinger på deres funktionelle mål, nogle gange kaldet substrater. Dynamikken af di
Forskere afkoder dynamikken i den største proteinnedbrydende maskine i atomare detaljerKredit:CC0 Public Domain Protein nanomaskiner lavet af flere proteinmolekyler er meget dynamiske under deres handlinger på deres funktionelle mål, nogle gange kaldet substrater. Dynamikken af di
- Hvad har mere effekt på gravitationskraftmasse eller afstand?
- Fossilt bevis på dvale-lignende tilstand i 250 millioner år gammelt antarktisk dyr
- Selfies og sociale medier:Hvordan turister forkæler deres influencer-fantasier
- Strålingsdetekterende plastik får ingrediens til at forblive i det klare
- Hvilken enhed konverterer solenergi?
- Hvordan skaber solen energi, og hvor den sker?


