Sigma-bindinger i CH₂Cl₂:En detaljeret forklaring
Forstå Sigma-obligationer
* Sigma-bindinger (σ-bindinger) er den stærkeste type kovalente bindinger. De er dannet af den direkte overlapning af atomare orbitaler langs den internukleære akse.
* Enkeltobligationer er altid sigma-bindinger.
Analyse af molekylet
1. Central kulstof: Kulstofatomet i CH₂Cl₂ danner fire enkeltbindinger:
* To bindinger til hydrogenatomer (CH)
* To bindinger til kloratomer (C-Cl)
2. Brint og klor: Hvert brint- og chloratom danner en enkeltbinding (H-C og Cl-C).
Tælling af Sigma-obligationer
Derfor er der i alt 4 sigma-bindinger i CH2Cl2.
Sidste artikelFysisk vs. kemisk ændring:eksempler og definitioner
Næste artikelCobaltsulfat bliver blåt med NaOH:Kemisk reaktion forklaret
 Varme artikler
Varme artikler
-
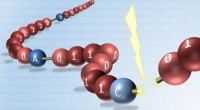 Verdens første til at læse digitalt kodede syntetiske molekylerVed at indsætte skrøbelige bindinger mellem hver molekylær byte, digitale polymerer kan let aflæses gennem massespektrometri. Kredit:Jean-François Lutz, Institut Charles Sadron (CNRS) Ved hjælp af
Verdens første til at læse digitalt kodede syntetiske molekylerVed at indsætte skrøbelige bindinger mellem hver molekylær byte, digitale polymerer kan let aflæses gennem massespektrometri. Kredit:Jean-François Lutz, Institut Charles Sadron (CNRS) Ved hjælp af -
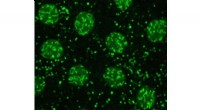 Lipiddråber spiller afgørende roller ud over fedtopbevaringForskerne brugte avanceret fluorescensmikroskopi til at se lipiddråber i frugtflueembryoner. Her, H2Av (fluoresceret i grønt) er til stede i cellens kerner (de store klatter) og på lipiddråber (de min
Lipiddråber spiller afgørende roller ud over fedtopbevaringForskerne brugte avanceret fluorescensmikroskopi til at se lipiddråber i frugtflueembryoner. Her, H2Av (fluoresceret i grønt) er til stede i cellens kerner (de store klatter) og på lipiddråber (de min -
 Hurtig test for at påvise salmonella i fødevarerTilfælde af salmonella-madforgiftning er et tilbagevendende fænomen. Råt kød er en hyppig smittekilde. Hvis rundstykket med svinetatar på billedet her var forurenet med patogener, at spise det kan før
Hurtig test for at påvise salmonella i fødevarerTilfælde af salmonella-madforgiftning er et tilbagevendende fænomen. Råt kød er en hyppig smittekilde. Hvis rundstykket med svinetatar på billedet her var forurenet med patogener, at spise det kan før -
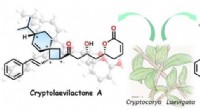 Australsk busk indeholder en ny klasse af organisk forbindelseIsolationer af unikke monoterpen-polyketider med spiro[3, 5]nonan fra C. laevigata . Kredit:Kanazawa University Den botaniske verden kan være et spændende sted for kemikere. Plantearter producer
Australsk busk indeholder en ny klasse af organisk forbindelseIsolationer af unikke monoterpen-polyketider med spiro[3, 5]nonan fra C. laevigata . Kredit:Kanazawa University Den botaniske verden kan være et spændende sted for kemikere. Plantearter producer
- Forudsige, hvordan nanopartikler vil reagere i den menneskelige krop
- Hvordan DNA-analyse af vores floder og søer kan afsløre nye hemmeligheder om deres biodiversitet
- Hvad forhindrer temperaturen i at blive for høj på varme steder?
- Droner til at spore en af de største dæmningsfjernelser på den østlige kyst
- Gratis vejledning til at lave et barometer
- At trodse en 150 år gammel regel for faseadfærd


