Cobaltsulfat bliver blåt med NaOH:Kemisk reaktion forklaret
1. Indledende løsning:
* Cobaltsulfat (CoSO4) i opløsning eksisterer som lyserøde hydratiserede cobalt(II)-ioner ([Co(H2O)6]²+).
2. Tilsætning af NaOH:
* Når du tilføjer NaOH, reagerer hydroxidionerne (OH⁻) fra NaOH med de hydrerede kobolt(II)-ioner.
3. Kompleks iondannelse:
* Denne reaktion får nogle af de vandmolekyler, der omgiver cobalt(II)-ionen, til at blive erstattet af hydroxidioner. Dette resulterer i dannelsen af en blå tetraedrisk kompleksion:[Co(OH)4]²⁻.
4. Farveændring:
* Forskellen i farve mellem den lyserøde hydratiserede kobolt(II)-ion og den blå tetraedriske kompleksion skyldes ændringen i koordinationsmiljøet omkring koboltatomet. De forskellige ligander (vand vs. hydroxid) påvirker måden koboltatomet absorberer og udsender lys.
Opsummering:
Tilsætning af NaOH til koboltsulfatopløsning forårsager en farveændring fra pink til blå, fordi det fører til dannelsen af en blå tetraedrisk kompleksion, [Co(OH)₄]²⁻, ved at erstatte nogle af de vandmolekyler, der omgiver cobalt(II)-ionen, med hydroxidioner.
Sidste artikelSigma-bindinger i CH₂Cl₂:En detaljeret forklaring
Næste artikelHydrogenperoxid pH:Forståelse af surhed og koncentration
 Varme artikler
Varme artikler
-
 Effektive måder at fjerne totalt opløste faste stoffer (TDS) fra drikkevandAf Michael Rytting Opdateret 24. marts 2022 Total Dissolved Solids (TDS) omfatter de mineralske og kemiske rester, der forbliver i vandet efter konventionel filtrering. Mens de fleste husholdningsfi
Effektive måder at fjerne totalt opløste faste stoffer (TDS) fra drikkevandAf Michael Rytting Opdateret 24. marts 2022 Total Dissolved Solids (TDS) omfatter de mineralske og kemiske rester, der forbliver i vandet efter konventionel filtrering. Mens de fleste husholdningsfi -
 Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m
Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m -
 Forskere opdager en forbindelse mellem to vigtige produkter af nitrogenoxidEksperimenter afslører en hidtil ukendt mekanisme, der ligger til grund for dannelsen af nitrosothioler. Kredit:Daniela Ramos Truzzi Lige siden tre amerikansk-baserede forskere, der arbejder uaf
Forskere opdager en forbindelse mellem to vigtige produkter af nitrogenoxidEksperimenter afslører en hidtil ukendt mekanisme, der ligger til grund for dannelsen af nitrosothioler. Kredit:Daniela Ramos Truzzi Lige siden tre amerikansk-baserede forskere, der arbejder uaf -
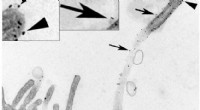 Downstream-signalering:Cilia frigiver ektosomer for at levere vigtige beskeder i nyrenImmunogold mærkning af Exoc5-myc (en komponent i eksocysten) i MDCK-celler viser sorte prikker langs det primære cilium (pilespidser) og tilhørende vesikler (pile). Billedet er taget ved 53, 400X fors
Downstream-signalering:Cilia frigiver ektosomer for at levere vigtige beskeder i nyrenImmunogold mærkning af Exoc5-myc (en komponent i eksocysten) i MDCK-celler viser sorte prikker langs det primære cilium (pilespidser) og tilhørende vesikler (pile). Billedet er taget ved 53, 400X fors


