Beregning af HCl-volumen for Ba(OH)₂-neutralisering:En trin-for-trin guide
1. Skriv den afbalancerede kemiske ligning:
2HCl(aq) + Ba(OH)2(aq) → BaCl2(aq) + 2H2O(l)
2. Bestem molforholdet:
Fra den afbalancerede ligning ser vi, at 2 mol HCl reagerer med 1 mol Ba(OH)2.
3. Beregn mol af Ba(OH)₂:
* Konverter rumfanget af Ba(OH)₂ til dm³:25,0 cm³ =0,025 dm³
* Mol af Ba(OH)2 =koncentration × volumen
* Mol af Ba(OH)2 =0,200 mol/dm³ × 0,025 dm³ =0,005 mol
4. Beregn de nødvendige mol HCl:
* Da molforholdet er 2:1, har vi brug for dobbelt så mange mol HCl:
* Mol HCl =0,005 mol Ba(OH)2 x (2 mol HCl / 1 mol Ba(OH)2) =0,010 mol HCl
5. Beregn volumen af HCl:
* Volumen af HCl =mol HCl / koncentration af HCl
* Volumen af HCl =0,010 mol / 0,200 mol/dm³ =0,050 dm³
6. Konverter til cm³:
* Volumen af HCl =0,050 dm³ × (1000 cm³ / 1 dm³) =50 cm³
Derfor kræves 50 cm³ 0,200 mol/dm³ HCl for at neutralisere 25,0 cm³ af 0,200 mol/dm³ Ba(OH)₂.
Sidste artikelEddike pH:Forstå surhed og pH-skalaen
Næste artikelPenny in Gold Lab:Hvad sker der virkelig med kobberet?
 Varme artikler
Varme artikler
-
 Happy hour for tidsopløst krystallografiLiquid Application Method for time-resolved Analyses (LAMA) åbner døren for alle diffusionsvenlige proteinkrystalsystemer. Kredit:Joerg M. Harms, MPSD Forskere fra Department of Atomically Resolve
Happy hour for tidsopløst krystallografiLiquid Application Method for time-resolved Analyses (LAMA) åbner døren for alle diffusionsvenlige proteinkrystalsystemer. Kredit:Joerg M. Harms, MPSD Forskere fra Department of Atomically Resolve -
 Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata -
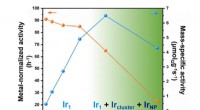 Højbelastende atomisk dispergeret Ir/MoC-katalysator til hydrogeneringsreaktionMetalnormaliseret aktivitet og massespecifik aktivitet af Ir/MoC-katalysatorer med forskelligt Ir-indhold. Ir1 står for atomically dispersed Ir. Skyggen fremhæver, at når Ir -belastningen er lavere en
Højbelastende atomisk dispergeret Ir/MoC-katalysator til hydrogeneringsreaktionMetalnormaliseret aktivitet og massespecifik aktivitet af Ir/MoC-katalysatorer med forskelligt Ir-indhold. Ir1 står for atomically dispersed Ir. Skyggen fremhæver, at når Ir -belastningen er lavere en -
 Terminatorlignende flydende metal bevæger sig og strækker sig i 3D-rumKredit:American Chemical Society I blockbusteren Terminator film franchise, en ond robot forvandler sig til forskellige menneskelige former og objekter og oser gennem smalle åbninger, takket vær
Terminatorlignende flydende metal bevæger sig og strækker sig i 3D-rumKredit:American Chemical Society I blockbusteren Terminator film franchise, en ond robot forvandler sig til forskellige menneskelige former og objekter og oser gennem smalle åbninger, takket vær
- Hvordan ved du, hvorfor termisk energi ved at brænde matchstick?
- Hvorfor studerer astronomer en gruppe stjerner snarere end kun en stjerne, når de studerer livscykl…
- Sådan træner du din robot:Forskning giver nye tilgange
- Marine hedebølger har ødelæggende indvirkning på livet i havet i det tropiske vestlige og centra…
- Hvilken type celler er kendt som gameter?
- Hvilken slags energi kan ændre sig til en anden energi?


