Støkiometriproblem:Beregning af produktudbytte i en kemisk reaktion
1. Afbalanceret kemisk ligning
Den angivne ligning er ikke afbalanceret:
2A3 + 3B2 → 6AB
For at afbalancere det skal vi sikre, at antallet af atomer i hvert grundstof er det samme på begge sider af ligningen.
* A-atomer: Der er 6 A-atomer til venstre (2 x 3) og 6 A-atomer til højre.
* B-atomer: Der er 6 B-atomer til venstre (3 x 2) og 6 B-atomer til højre.
Ligningen er allerede afbalanceret!
2. Moleforhold
Den afbalancerede ligning fortæller os molforholdet mellem reaktanter og produkter. Fra den balancerede ligning:
* 2 mol A3 reagerer med 3 mol B2 for at producere 6 mol AB
3. Begrænsende reaktant
Vi får at vide, at 10 mol A3 reageres med overskydende B2. Det betyder, at A3 er den begrænsende reaktant. Den begrænsende reaktant er den, der bliver brugt op først og bestemmer mængden af dannet produkt.
4. Beregning af mol af AB
Da molforholdet er 2 mol A3 :6 mol AB, kan vi opstille en andel:
* 2 mol A3 / 6 mol AB =10 mol A3 / x mol AB
Løsning for x:
* x =(10 mol A3 * 6 mol AB) / 2 mol A3
* x =30 mol AB
Svar: Hvis 10 mol A3 omsættes med overskydende B2, vil der blive produceret 30 mol AB.
Sidste artikelAtommodeller vs. rigtige atomer:Forstå forskellen
Næste artikelBeregning af mol af ilt i kuldioxid:en trin-for-trin guide
 Varme artikler
Varme artikler
-
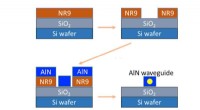 Forskere reducerer drastisk teknologi til fingeraftryk af lægemidler og andre kemikalierSkematisk, der viser trinene til oprettelse af den optiske bølgeleder. Kredit:Texas A&M University College of Engineering Efterhånden som nye infektionssygdomme opstår og spredes, et af de bedste
Forskere reducerer drastisk teknologi til fingeraftryk af lægemidler og andre kemikalierSkematisk, der viser trinene til oprettelse af den optiske bølgeleder. Kredit:Texas A&M University College of Engineering Efterhånden som nye infektionssygdomme opstår og spredes, et af de bedste -
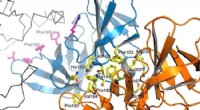 Nyt mål for udvikling af innovative antibiotikaBrasilianske og franske videnskabsmænd viser, at inhibering af interaktionen mellem to nøgleproteiner til cellevægsforlængelse kan være en effektiv strategi til at dræbe bakterier af bacillus-typen. K
Nyt mål for udvikling af innovative antibiotikaBrasilianske og franske videnskabsmænd viser, at inhibering af interaktionen mellem to nøgleproteiner til cellevægsforlængelse kan være en effektiv strategi til at dræbe bakterier af bacillus-typen. K -
 3 videnskabsbaserede tips til at løfte din Thanksgiving-middagFoxys_forest_manufacture/iStock/GettyImages Når Thanksgiving nærmer sig, bekymrer mange af os os om at levere en fejlfri fest. Mens ferien er gennemsyret af tradition, kan videnskaben bag madlavning
3 videnskabsbaserede tips til at løfte din Thanksgiving-middagFoxys_forest_manufacture/iStock/GettyImages Når Thanksgiving nærmer sig, bekymrer mange af os os om at levere en fejlfri fest. Mens ferien er gennemsyret af tradition, kan videnskaben bag madlavning -
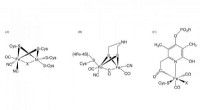 CO-biosyntese påkrævet til samling af det aktive sted i NiFe-hydrogenaseFigur 1. Struktur af de aktive steder i [NiFe] -hydrogenase, [FeFe] -hydrogenase, og [Fe] -hydrogenase Kredit:NINS/IMS En forskergruppe, der omfatter forskere fra Exploratory Research Center on Li
CO-biosyntese påkrævet til samling af det aktive sted i NiFe-hydrogenaseFigur 1. Struktur af de aktive steder i [NiFe] -hydrogenase, [FeFe] -hydrogenase, og [Fe] -hydrogenase Kredit:NINS/IMS En forskergruppe, der omfatter forskere fra Exploratory Research Center on Li
- Hvilken egenskab ved stof måles i kubisk centimeter?
- Hawkings sidste bog giver korte svar på store spørgsmål
- Hvorfor tørrede Mars ud? Ny undersøgelse peger på usædvanlige svar
- Hvordan påvirker træer vejret?
- Hvilke problemer skal overvindes, før fusion kan bruges til at producere energi?
- Hvilke molekyler udgør nucliecsyrer?


