Forståelse af atomvolumen:et kvantemekanisk perspektiv
* Uklare grænser: Atomer har ikke hårde, veldefinerede kanter som en solid bold. Elektronskyen, der omgiver kernen, er en sandsynlighedsfordeling – det er mere som et diset, konstant fluktuerende område, hvor der sandsynligvis vil blive fundet elektroner.
* Kvantemekanik: Elektronernes adfærd i atomer er styret af kvantemekanik, som beskriver deres bølgelignende natur. Det betyder, at deres positioner ikke er præcist definerede, hvilket gør det vanskeligt at tildele en fast lydstyrke.
I stedet for en fast lydstyrke taler vi ofte om:
* Atomradius: Dette er et mål for den gennemsnitlige afstand fra kernen til den yderste elektron. Det kan beregnes ved hjælp af forskellige metoder, men det er stadig en omtrentlig værdi.
* Van der Waals Radius: Dette repræsenterer afstanden mellem to ikke-bundne atomer, når de er tættest på hinanden. Det er nyttigt til at forstå, hvordan atomer pakkes sammen i molekyler og faste stoffer.
* Effektiv nuklear ladning: Dette koncept overvejer, hvordan kernens positive ladning "føles" af elektronerne under hensyntagen til afskærmning fra andre elektroner. Det påvirker størrelsen af atomet.
Så kort sagt er der ikke noget enkelt, universelt accepteret "volumen" af et atom. I stedet bruger vi forskellige modeller og målinger til at beskrive dens størrelse og den plads, som dens elektronsky optager.
 Varme artikler
Varme artikler
-
 Hvad er en organisk forbindelse? – Definition, typer og livets byggestenMariemlulu/iStock/GettyImages TL;DR En organisk forbindelse er et kemikalie, der indeholder kulstofatomer bundet af kovalente forbindelser til andre grundstoffer såsom brint, oxygen, nitrogen og lejl
Hvad er en organisk forbindelse? – Definition, typer og livets byggestenMariemlulu/iStock/GettyImages TL;DR En organisk forbindelse er et kemikalie, der indeholder kulstofatomer bundet af kovalente forbindelser til andre grundstoffer såsom brint, oxygen, nitrogen og lejl -
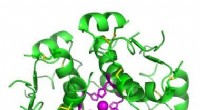 Forskere bruger zink til at målrette insulinproducerende celler med regenerativ medicinHøjopløsningsmodel af seks insulinmolekyler samlet i en hexamer. Kredit:Isaac Yonemoto/Wikipedia En insulininjektion kan håndtere diabetessymptomer, men faktisk at helbrede sygdommen ville betyde
Forskere bruger zink til at målrette insulinproducerende celler med regenerativ medicinHøjopløsningsmodel af seks insulinmolekyler samlet i en hexamer. Kredit:Isaac Yonemoto/Wikipedia En insulininjektion kan håndtere diabetessymptomer, men faktisk at helbrede sygdommen ville betyde -
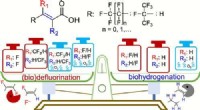 Under anaerobe forhold kan almindelige mikrobielle samfund bryde den ultra-stærke kulstof-fluor-bin…Kredit:Yaochun Yu et al., Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c05509 Ingeniører ved University of California Riverside er de første til at rapportere selektiv nedbrydning
Under anaerobe forhold kan almindelige mikrobielle samfund bryde den ultra-stærke kulstof-fluor-bin…Kredit:Yaochun Yu et al., Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c05509 Ingeniører ved University of California Riverside er de første til at rapportere selektiv nedbrydning -
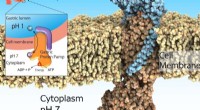 Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s
Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s
- Boeing Starliner-bemandet mission udskudt til mindst fredag
- Jordens fryse-optøning stimulerer udledning af lattergas fra alpine enge
- Hvilke mineralressourcer kan høstes fra kontinentalsokklen?
- Revidering af klimamodeller med nye aerosolfeltdata
- Hvad er den afbalancerede ligning, når sølv og svovl S8 reagerer?
- Insect Compound Eye vs Human Eye


