Beregning af hydrogenionkoncentration ([H+]) fra myresyreopløsning - trin-for-trin
1. Forstå konceptet
* Myresyre (HCOOH) er en svag syre. Det betyder, at det ikke ioniseres fuldstændigt i vand. Vi skal bruge dens Ka-værdi til at finde [H+].
* Ka (syredissociationskonstant) er et mål for, hvor meget en syre ioniserer i vand. Jo lavere Ka, jo svagere er syren.
2. Den kemiske reaktion
Myresyre dissocierer i vand i overensstemmelse med denne ligevægt:
HCOOH(aq) ⇌ H+(aq) + HCOO-(aq)
3. Opsætning af ICE-bordet
Vi bruger en ICE-tabel (Initial, Change, Equilibrium) til at beregne ligevægtskoncentrationerne:
| | HCOOH | H+ | HCOO- |
|-------------|--------|-------|--------|
| Indledende | 0,35 M | 0 | 0 |
| Skift | -x | +x | +x |
| Ligevægt | 0,35-x| x | x |
4. Ka-udtrykket
Ka-udtrykket for myresyre er:
Ka =[H+][HCOO-] / [HCOOH]
Ka-værdien for myresyre er 1,8 x 10^-4
5. Løs for x
Erstat ligevægtskoncentrationerne fra ICE-tabellen med Ka-udtrykket:
1,8 x 10^-4 =(x)(x) / (0,35 - x)
Da Ka er lille, kan vi antage, at x er meget mindre end 0,35, så vi kan forenkle:
1,8 x 10^-4 =x^2 / 0,35
Løs for x:
x^2 =6,3 x 10^-5
x =0,0079 M
6. Svaret
Da x repræsenterer koncentrationen af H+ ioner:
[H+] =0,0079 M
Vigtig bemærkning: Dette svar er en tilnærmelse. For mere nøjagtige resultater skal den andengradsligning bruges til at løse for x.
Sidste artikelForståelse af kemiske forbindelser:Definition og eksempler
Næste artikelForståelse af atomvolumen:et kvantemekanisk perspektiv
 Varme artikler
Varme artikler
-
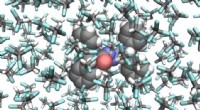 Forskere laver en fotografisk film af en molekylær switchMolekylær struktur af den fotoresponsive molekylære switch (i midten) omgivet af opløsningsmiddelmolekyler. Forskerne afslørede en lys-induceret pedalo-type bevægelse, som går både frem og tilbage. Bi
Forskere laver en fotografisk film af en molekylær switchMolekylær struktur af den fotoresponsive molekylære switch (i midten) omgivet af opløsningsmiddelmolekyler. Forskerne afslørede en lys-induceret pedalo-type bevægelse, som går både frem og tilbage. Bi -
 Egenskaber af katalysatorer studeret med gammastråleresonansKredit:Kazan Federal University Dampstøttede olieudvindingsmetoder til tunge aflejringer har længe været i fokus på Kazan Federal University. I særdeleshed, Der lægges stor vægt på in-situ forbræn
Egenskaber af katalysatorer studeret med gammastråleresonansKredit:Kazan Federal University Dampstøttede olieudvindingsmetoder til tunge aflejringer har længe været i fokus på Kazan Federal University. I særdeleshed, Der lægges stor vægt på in-situ forbræn -
 Selvsamling påkrævet:Neutrons sonde ny polymeradfærd for biomedicinske materialerORNL-instrumentforsker Shuo Qian forbereder Bio-SANS-instrumentet på HFIR til et eksperiment ledet af LSU-professor Donghui Zhang. Zhang bruger neutronspredning til at studere alsidige proteinlignende
Selvsamling påkrævet:Neutrons sonde ny polymeradfærd for biomedicinske materialerORNL-instrumentforsker Shuo Qian forbereder Bio-SANS-instrumentet på HFIR til et eksperiment ledet af LSU-professor Donghui Zhang. Zhang bruger neutronspredning til at studere alsidige proteinlignende -
 Fjernelse af kuldioxid fra kraftværkets udstødningMIT assisterende professor Betar Gallant (til venstre) og kandidatstuderende Aliza Khurram er ved at udvikle et nyt batteri, der både kan fange kuldioxid i kraftværkets udstødning og omdanne det til e
Fjernelse af kuldioxid fra kraftværkets udstødningMIT assisterende professor Betar Gallant (til venstre) og kandidatstuderende Aliza Khurram er ved at udvikle et nyt batteri, der både kan fange kuldioxid i kraftværkets udstødning og omdanne det til e
- Hvilke egenskaber gør en organisme protist?
- Hvad er den videnskabelige undersøgelse af strukturen, hvis jorden?
- Nebra Sky Disc:Tidlig kalender,
- Er det sandt eller falsk, at mennesker ikke har stor indflydelse på miljøet?
- En global bevægelsesplanlægningstilgang baseret på lokale erfaringer
- Hvilket lag er under jorden, hvor der ikke er tomme rum for vand eller luft at udfylde?


