Beregning af CO2-produktion fra ethanforbrænding:En trin-for-trin guide
1. Skriv den afbalancerede kemiske ligning:
Forbrændingen af ethan (C₂H6) med oxygen (O₂) producerer kuldioxid (CO₂) og vand (H₂O):
2 C₂H6 + 7 O₂ → 4 CO₂ + 6 H₂O
2. Bestem molforholdet:
Den afbalancerede ligning viser, at for hver 2 mol brændt ethan, produceres 4 mol CO₂.
3. Beregn antallet af producerede mol CO₂:
Brug af molforholdet fra den balancerede ligning:
(5,60 mol C2H6) * (4 mol CO2 / 2 mol C2H6) =11,2 mol CO2
Derfor produceres 11,2 mol CO₂, når 5,60 mol ethan forbrændes i overskydende ilt.
Sidste artikelAmmoniakbindinger:Forståelse af polaritet og elektronegativitet
Næste artikelJernionladning i Fe₂O₃:En detaljeret forklaring
 Varme artikler
Varme artikler
-
 Håndholdt spektralanalysator gør smartphonen til et diagnostisk værktøjDen spektrale transmissions-reflektans-intensitet (TRI) -analysator fastgøres til en smartphone og analyserer patientblod, urin, eller spytprøver lige så pålideligt som klinikbaserede instrumenter, de
Håndholdt spektralanalysator gør smartphonen til et diagnostisk værktøjDen spektrale transmissions-reflektans-intensitet (TRI) -analysator fastgøres til en smartphone og analyserer patientblod, urin, eller spytprøver lige så pålideligt som klinikbaserede instrumenter, de -
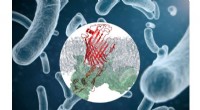 Ny funktionel indsigt i proteinkompleks, muligt nyt mål for antibiotikaProteinkomplekset (rødt) i bakteriens ydre membran. Kredit:Utrecht University Faculty of Science Forskere ved Utrecht Universitet har fået ny indsigt i strukturen og funktionen af et proteinkomp
Ny funktionel indsigt i proteinkompleks, muligt nyt mål for antibiotikaProteinkomplekset (rødt) i bakteriens ydre membran. Kredit:Utrecht University Faculty of Science Forskere ved Utrecht Universitet har fået ny indsigt i strukturen og funktionen af et proteinkomp -
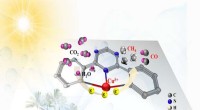 Ny katalysator øger radikalt omdannelseshastigheden af kuldioxid til solbrændstofferForskere konstruerede en enkelt atom katalysator (SAC) med en kovalent triazin-baseret ramme, hvormed fotokatalytisk CO2 blev omdannet til solenergi. Den fremstillede fotokatalysator udviste fremragen
Ny katalysator øger radikalt omdannelseshastigheden af kuldioxid til solbrændstofferForskere konstruerede en enkelt atom katalysator (SAC) med en kovalent triazin-baseret ramme, hvormed fotokatalytisk CO2 blev omdannet til solenergi. Den fremstillede fotokatalysator udviste fremragen -
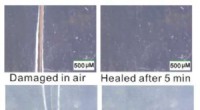 Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
- Hvad er en kosmisk ko?
- Fællesskabet siger modvilligt farvel til det 600 år gamle træ
- Svaret på jobstress? Hvorfor, et kæledyr!
- Vild druegær kunne være mere effektiv end pesticider til at forhindre druemug
- Hvad gør hastigheden os i stand til at gøre?
- Facebook-hack afslører farerne ved at bruge en enkelt konto til at logge ind på andre tjenester


