Ammoniakbindinger:Forståelse af polaritet og elektronegativitet
* Elektronegativitetsforskel: Nitrogen (N) har en højere elektronegativitet end brint (H). Dette betyder, at nitrogen tiltrækker de delte elektroner i N-H-bindingerne stærkere.
* Ulige deling: Den ulige deling af elektroner resulterer i en delvis negativ ladning (δ-) på nitrogenatomet og delvise positive ladninger (δ+) på brintatomerne.
* Dipolmoment: Denne ujævne fordeling af ladningen skaber et permanent dipolmoment i ammoniakmolekylet, hvilket gør bindingerne polære kovalente.
Opsummering: Forskellen i elektronegativitet mellem nitrogen og brint fører til polære kovalente bindinger i ammoniak, hvor nitrogenatomet har en delvis negativ ladning og brintatomerne har delvist positive ladninger.
 Varme artikler
Varme artikler
-
 Oprettelse af mRNA med en helt kemisk proces kan give mulighed for tilpassede mRNA-vaccinermRNA med sin glødende hætte. Kredit:Reiko Matsushita Forskere ved Nagoya University i Japan har udviklet en ny kemisk proces, der kan repræsentere et vigtigt gennembrud i at skabe skræddersyede mRN
Oprettelse af mRNA med en helt kemisk proces kan give mulighed for tilpassede mRNA-vaccinermRNA med sin glødende hætte. Kredit:Reiko Matsushita Forskere ved Nagoya University i Japan har udviklet en ny kemisk proces, der kan repræsentere et vigtigt gennembrud i at skabe skræddersyede mRN -
 Hvordan langvarig strålingseksponering skader atomreaktorerKredit:CC0 Public Domain Ny forskning fra Texas A&M University-forskere kan hjælpe med at øge effektiviteten af atomkraftværker i den nærmeste fremtid. Ved at bruge en kombination af fysikbaseret
Hvordan langvarig strålingseksponering skader atomreaktorerKredit:CC0 Public Domain Ny forskning fra Texas A&M University-forskere kan hjælpe med at øge effektiviteten af atomkraftværker i den nærmeste fremtid. Ved at bruge en kombination af fysikbaseret -
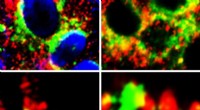 Undersøgelse afslører potentielt nyt behandlingsmål i kampen mod COVID-19Celler, der viser tæt nærhed (gul) af GRP78 (grøn) med Spike-protein af SARS-Cov-2 (rød) (venstre paneler) og ACE2 (rød) (højre paneler). Kredit:Hovedforfatter Anthony Carlos, PhD Den hurtige udvi
Undersøgelse afslører potentielt nyt behandlingsmål i kampen mod COVID-19Celler, der viser tæt nærhed (gul) af GRP78 (grøn) med Spike-protein af SARS-Cov-2 (rød) (venstre paneler) og ACE2 (rød) (højre paneler). Kredit:Hovedforfatter Anthony Carlos, PhD Den hurtige udvi -
 Team udvikler ny halvlederbehandlingsteknologiEn konstruktion designet på en sådan måde, at kun grønt lys må passere. Kredit:TU Wien Ekstremt fine porøse strukturer med bittesmå huller, ligner en slags svamp på nanoniveau, kan genereres i hal
Team udvikler ny halvlederbehandlingsteknologiEn konstruktion designet på en sådan måde, at kun grønt lys må passere. Kredit:TU Wien Ekstremt fine porøse strukturer med bittesmå huller, ligner en slags svamp på nanoniveau, kan genereres i hal
- Forskere finder utætte apps, der udsætter privatlivets fred
- Økonomiske skader kunne være værre uden lockdown og social distancering, undersøgelse finder
- En vulkan dannet over tid fra tusinder af lavaudbrud, der deponerer lag efter ny skorpe?
- Hvilken faktor har den største indflydelse på forvitringshastigheden på jordoverfladen?
- Hvornår forventes en aseriod næste gang at ramme jorden?
- Er en lagring af gravitationspotentiale energi?


