Nitrogenoxidationstal:Forståelse -3 og videre
Her er hvorfor:
* Nitrogens elektronkonfiguration: Nitrogen har 5 valenselektroner. For at opnå en stabil oktet ønsker den at få 3 elektroner mere.
* Danning af negative ioner: Når nitrogen får 3 elektroner, danner det en nitridion (N³⁻), hvilket resulterer i et oxidationstal på -3.
* Eksempler: Denne oxidationstilstand ses i forbindelser som ammoniak (NH3) og nitrider (f.eks. Mg3N2).
Mens -3 er den mest almindelige, kan nitrogen udvise andre oxidationstilstande, der spænder fra -3 til +5, afhængigt af det kemiske miljø.
 Varme artikler
Varme artikler
-
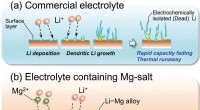 Forskere tager skridt mod sikrere batterier ved at trimme litiumgreneSkematisk illustration af den foreslåede undertrykkende effekt af Li dendritisk vækst ved tilsætning af Mg-salt. Kredit:Royal Society of Chemistry Et samarbejdende team af forskere fra Shinshu Uni
Forskere tager skridt mod sikrere batterier ved at trimme litiumgreneSkematisk illustration af den foreslåede undertrykkende effekt af Li dendritisk vækst ved tilsætning af Mg-salt. Kredit:Royal Society of Chemistry Et samarbejdende team af forskere fra Shinshu Uni -
 Nyopdaget enzym bruger en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugtKredit:CC0 Public Domain Nyopdaget enzym anvender en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugt i øjnene Det ildelugtende molekyle, der giver husdyrgødning sin frast
Nyopdaget enzym bruger en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugtKredit:CC0 Public Domain Nyopdaget enzym anvender en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugt i øjnene Det ildelugtende molekyle, der giver husdyrgødning sin frast -
 Vejskilte for immunforsvarscellerKredit:CC0 Public Domain Organismer bliver konstant invaderet af patogener såsom vira. Vores immunsystem går i gang for at bekæmpe disse patogener med det samme. Det medfødte uspecifikke immunrespo
Vejskilte for immunforsvarscellerKredit:CC0 Public Domain Organismer bliver konstant invaderet af patogener såsom vira. Vores immunsystem går i gang for at bekæmpe disse patogener med det samme. Det medfødte uspecifikke immunrespo -
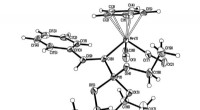 Kemikere opdager en ny dannelsesmekanisme for kræftbekæmpende stofferEt af cymantrenderivaterne, der blev brugt i undersøgelsen. Kredit:Alexander Smolyakov RUDN Universitets kemikere reviderede dannelsesmekanismen for organofosforkomplekser med metal. Resultaterne
Kemikere opdager en ny dannelsesmekanisme for kræftbekæmpende stofferEt af cymantrenderivaterne, der blev brugt i undersøgelsen. Kredit:Alexander Smolyakov RUDN Universitets kemikere reviderede dannelsesmekanismen for organofosforkomplekser med metal. Resultaterne
- Hvordan undersøgelser af tendenser i menneskelig levetid kan måle fremskridt i forhold til ulighed…
- Pandemi viser, at centralbanker kan være bedre stillet til at arbejde sammen
- Video:Hvordan tåregas påvirker din krop
- Hvordan er organiske forbindelser og levende ting relateret?
- Coenzymes rolle
- Landbrugets hemmelige våben:styrkelse af kvinder


