Mestring af kemiske ligninger:En omfattende guide til balancering
Sådan løses kemiske ligninger:En trin-for-trin guide
Afbalancering af kemiske ligninger er afgørende for nøjagtigt at repræsentere kemiske reaktioner. Her er en oversigt over processen:
1. Identificer reaktanterne og produkterne:
* Reaktanter: De stoffer, der er til stede i begyndelsen af reaktionen. Disse er skrevet i venstre side af ligningen.
* Produkter: De stoffer, der dannes som følge af reaktionen. Disse er skrevet i højre side af ligningen.
2. Skriv den ubalancerede ligning:
* Brug de kemiske formler for reaktanterne og produkterne, adskilt af et plustegn (+) på hver side af ligningen.
* Brug en pil (→) til at adskille reaktanterne fra produkterne.
Eksempel: Ubalanceret ligning:
* H2 + O2 → H2O
3. Balancer ligningen:
* Loven om messens bevarelse: Denne lov siger, at i et lukket system skal den samlede masse af reaktanterne før en kemisk reaktion svare til den samlede masse af produkterne efter reaktionen.
* Koefficienter: Disse er hele tal placeret foran hver kemisk formel. De repræsenterer antallet af molekyler eller mol af hvert stof involveret i reaktionen.
* Abonnementer: Disse er små tal skrevet under og til højre for et elements symbol. De angiver antallet af atomer af det element i et molekyle. Du kan ikke ændre subscripts for at balancere en ligning.
4. Balancering ved prøve og fejl:
* Start med det mest komplekse molekyle: Se efter molekylet med flest atomer eller den mest komplekse struktur.
* Juster koefficienterne: Begynd med det mest komplekse molekyle og skift koefficienten foran det for at afbalancere antallet af atomer af det element på begge sider af ligningen.
* Balancer resten: Gentag processen for hvert element, indtil alle atomer på begge sider af ligningen er afbalancerede.
Eksempel:Afbalancering af ligningen for reaktionen mellem brint og ilt
1. Ubalanceret ligning: H2 + O2 -> H2O
2. Balancer ilt: Der er 2 oxygenatomer på venstre side (O₂) og 1 til højre (H₂O). Vi skal tilføje en koefficient på 2 foran H₂O:
* H2 + O2 → 2 H2O
3. Balancer brint: Der er 2 hydrogenatomer på venstre side (H2) og 4 på højre side (2H2O). Vi skal tilføje en koefficient på 2 foran H₂:
* 2 H2 + O2 -> 2H20
4. Balanceret ligning: 2 H2 + O2 → 2 H2O
Yderligere tip:
* Hold det enkelt: Fokuser på at balancere et element ad gangen.
* Giv ikke op: Det kan tage flere forsøg at finde de rigtige koefficienter.
* Dobbelttjek dit arbejde: Sørg for, at antallet af atomer i hvert grundstof er det samme på begge sider af ligningen.
Husk: Balancering af kemiske ligninger er en færdighed, der forbedres med øvelse. Fortsæt med at øve dig, så får du styr på det!
Sidste artikelCu+-kationelektron- og protonantal:En detaljeret forklaring
Næste artikelNitrogenoxidationstal:Forståelse -3 og videre
 Varme artikler
Varme artikler
-
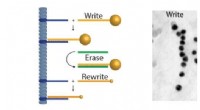 DNA som en supramolekylær byggestenKredit:Leiden Universitet Ph.d.-studerende Willem Noteborn har undersøgt supramolekylære strukturer. Disse kan være nyttige til indlæsning af medicin og signalmolekyler vedr. for eksempel, cellulæ
DNA som en supramolekylær byggestenKredit:Leiden Universitet Ph.d.-studerende Willem Noteborn har undersøgt supramolekylære strukturer. Disse kan være nyttige til indlæsning af medicin og signalmolekyler vedr. for eksempel, cellulæ -
 Modificerede biomaterialer samles selv på temperaturangivelserSelvsamlede strukturer dannet af fedtsyremodificerede elastinlignende polypeptider (FAME). Forskere bruger temperatursignaler til at få molekylerne til at samle sig selv. Kredit:Davoud Mozhdehi og Kel
Modificerede biomaterialer samles selv på temperaturangivelserSelvsamlede strukturer dannet af fedtsyremodificerede elastinlignende polypeptider (FAME). Forskere bruger temperatursignaler til at få molekylerne til at samle sig selv. Kredit:Davoud Mozhdehi og Kel -
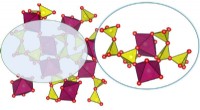 En overlegen, lavpris katalysator til vandspaltningStruktur af NaCo (PO3) 3metaphosphat med et udvidet billede af hjørnedelings [CoO6] octahedra og [PO4] tetraeder byggesten. Kredit:Indian Institute of Science I et væsentligt skridt mod storstilet
En overlegen, lavpris katalysator til vandspaltningStruktur af NaCo (PO3) 3metaphosphat med et udvidet billede af hjørnedelings [CoO6] octahedra og [PO4] tetraeder byggesten. Kredit:Indian Institute of Science I et væsentligt skridt mod storstilet -
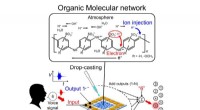 Intelligens, der kommer fra tilfældige polymernetværkStemmegenkendelse ved hjælp af sulfoneret polyanilin. Kredit:Creative Commons CC-BY, kredit:2021, Yuki Usami et al., Avancerede materialer Reservoir computing (RC) tackler komplekse problemer ved
Intelligens, der kommer fra tilfældige polymernetværkStemmegenkendelse ved hjælp af sulfoneret polyanilin. Kredit:Creative Commons CC-BY, kredit:2021, Yuki Usami et al., Avancerede materialer Reservoir computing (RC) tackler komplekse problemer ved
- Er tyngdekraften en kraftmasseafstand?
- Hvordan et usædvanligt varmt Indiske Ocean forårsagede oversvømmelser på Yangtze-floden
- Hvad påvirker mængden af solenergi, et panel absorberer?
- Er benzen et kovalent fast stof eller molekylært fast stof?
- Hvorfor var der og rsquot de ti mindre satellitter, der blev opdaget, indtil en rumprobe?
- Hvad er det sidste kerneelement for en sollignende stjerne?


