Periode 3 Elementer og opløselighed i hexan:En detaljeret forklaring
Forståelse af opløselighed i hexan
Hexan (C6H14) er et ikke-polært opløsningsmiddel. Det betyder, at det opløser stoffer, der også er upolære eller har en upolær komponent. Her er hvordan opløseligheden af periode 3-elementer relaterer sig til dette princip:
* Natrium (Na), Magnesium (Mg), Aluminium (Al): Disse er metaller og danner ioniske forbindelser. Ioniske forbindelser er polære, hvilket gør dem uopløselige i hexan.
* Silicon (Si): Silicium er et metalloid og eksisterer som et fast netværk. Selvom det har en vis kovalent binding, holdes det primært sammen af stærke interatomiske kræfter. Dette gør det uopløseligt i hexan.
* Fosfor (P), Svovl (S), Klor (Cl): Disse elementer kan danne ikke-polære kovalente forbindelser. Nogle eksempler:
* Hvidt fosfor (P4) er et upolært molekyle og opløseligt i hexan.
* Elementært svovl (S8) er lidt opløselig i hexan.
* Klor (Cl2) er et upolært diatomisk molekyle og opløseligt i hexan.
Vigtige overvejelser
* Oxidationstilstande: Et grundstofs opløselighed kan ændre sig afhængigt af dets oxidationstilstand. For eksempel er svovl i sin elementære form (S8) svagt opløselig, men svovl i sine oxidformer (som SO2) er polær og uopløselig i hexan.
* Specifikke forbindelser: Opløseligheden af specifikke forbindelser indeholdende periode 3-elementer vil afhænge af hele molekylets struktur og polaritet.
Opsummering: Grundstoffer i periode 3, der danner ikke-polære kovalente forbindelser, er sandsynligvis opløselige i hexan. Metaller, metalloider og ioniske forbindelser er generelt uopløselige.
 Varme artikler
Varme artikler
-
 Den hurtige fremtid for smarte stofferPå dette billede af stof, du kan se det grønne lys af funktionelle fibre. Ingen menneskeskabte genstande er mere allestedsnærværende eller udsat for mere vitale data end det tøj, vi alle bærer, siger
Den hurtige fremtid for smarte stofferPå dette billede af stof, du kan se det grønne lys af funktionelle fibre. Ingen menneskeskabte genstande er mere allestedsnærværende eller udsat for mere vitale data end det tøj, vi alle bærer, siger -
 Et nærmere kig på et magnesium viser, at meget små prøver er meget mere duktile end antagetIn situ TEM kompressionstest, der viser, at dislokationsglidning er ansvarlig for den plastiske deformation af en Mg enkeltkrystal søjle under c-akse kompression. (A) Sekskantet enhedscelle, der viser
Et nærmere kig på et magnesium viser, at meget små prøver er meget mere duktile end antagetIn situ TEM kompressionstest, der viser, at dislokationsglidning er ansvarlig for den plastiske deformation af en Mg enkeltkrystal søjle under c-akse kompression. (A) Sekskantet enhedscelle, der viser -
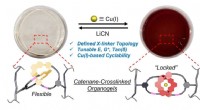 Sammenlåsende ringe låser op for nye materialeegenskaberAmatørkemikere husker måske, at kobber (Cu) normalt fremstår blåt i vand og grønt, når det er bundet af en standard ikke-aromatisk ligand. Men i tilfældet med de metalholdige catenaner, der er skabt i
Sammenlåsende ringe låser op for nye materialeegenskaberAmatørkemikere husker måske, at kobber (Cu) normalt fremstår blåt i vand og grønt, når det er bundet af en standard ikke-aromatisk ligand. Men i tilfældet med de metalholdige catenaner, der er skabt i -
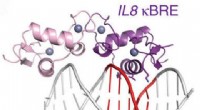 Duel af de inflammatoriske masterregulatorer – indsigt til lægemiddelopdagelseFigur:Diagram over glukokortikoidreceptoren, der binder et NF-kappaB-sted. Kredit:Hudson et al. Naturkommunikation (2018). Anti-inflammatoriske lægemidler såsom dexamethason kan have skadelige biv
Duel af de inflammatoriske masterregulatorer – indsigt til lægemiddelopdagelseFigur:Diagram over glukokortikoidreceptoren, der binder et NF-kappaB-sted. Kredit:Hudson et al. Naturkommunikation (2018). Anti-inflammatoriske lægemidler såsom dexamethason kan have skadelige biv
- Forskere finder, at 2-D overgangsmetalkarbider reagerer med vand, åbner en dør til deres ukendte k…
- Er en mikrobølgebutik elektricitet, når den er slukket?
- Hvorfor får du mere ATP ud af aerob respiration?
- Hvad er Bismuth -nitrat?
- Et spildt årti:Tiden tilbage til klimaindsats er skrumpet to tredjedele på 10 år
- For teatre, rise of streaming er en film, de har set før


