Ioniske vs. kovalente forbindelser:Nøgleforskelle forklaret
1. Obligationsdannelse:
* Ionisk: Dannet gennem overførslen af elektroner fra et metal til et ikke-metal. Dette skaber ioner med modsatte ladninger, der tiltrækker hinanden stærkt og danner en elektrostatisk binding.
* Kovalent: Dannet gennem delingen af elektroner mellem to ikke-metaller. Disse delte elektroner skaber en stabil, mere afbalanceret elektronkonfiguration for begge atomer.
2. Fysiske egenskaber:
* Ionisk: Typisk faste stoffer ved stuetemperatur med høje smelte- og kogepunkter . Det skyldes, at de stærke elektrostatiske kræfter kræver meget energi at overvinde. De er ofte skøre på grund af krystalgitterets stive struktur.
* Kovalent: Kan eksistere som faste stoffer, væsker eller gasser ved stuetemperatur, afhængigt af den specifikke forbindelse. Har generelt lavere smelte- og kogepunkter end ioniske forbindelser. De kan være fleksible på grund af obligationernes svagere karakter.
3. Opløselighed:
* Ionisk: Ofte opløseligt i vand på grund af den polære karakter af vandmolekyler, der er i stand til at interagere med de ladede ioner.
* Kovalent: Varieret i opløselighed hvor nogle er opløselige i vand (f.eks. sukkerarter) og andre er uopløselige (f.eks. olier). Opløseligheden afhænger af molekylets polaritet og vandmolekylernes evne til at danne brintbindinger.
Opsummering: Ioniske forbindelser dannes ved overførsel af elektroner, er normalt faste og stærke og opløses godt i vand. Kovalente forbindelser dannes ved deling af elektroner, kan eksistere i forskellige tilstande, har svagere bindinger og viser varierende opløselighed i vand.
 Varme artikler
Varme artikler
-
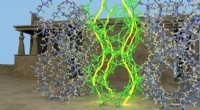 Kemiske karyatider forbedrer stabiliteten af metalorganiske rammerIllustration af de kemiske karyatider. Kredit:B. Smit/EPFL Metal-organiske rammer (MOFer) er materialer med porer i nanostørrelse i deres krystalstrukturer. Disse porer gør det muligt for MOFer at
Kemiske karyatider forbedrer stabiliteten af metalorganiske rammerIllustration af de kemiske karyatider. Kredit:B. Smit/EPFL Metal-organiske rammer (MOFer) er materialer med porer i nanostørrelse i deres krystalstrukturer. Disse porer gør det muligt for MOFer at -
 Udvikling af enzymer til at hjælpe med at løse planetens plastikproblemKredit:Unsplash/CC0 Public Domain Forskere fra Manchester Institute of Biotechnology (MIB) har udviklet en ny enzymteknologisk platform til at forbedre plastnedbrydende enzymer gennem rettet evolut
Udvikling af enzymer til at hjælpe med at løse planetens plastikproblemKredit:Unsplash/CC0 Public Domain Forskere fra Manchester Institute of Biotechnology (MIB) har udviklet en ny enzymteknologisk platform til at forbedre plastnedbrydende enzymer gennem rettet evolut -
 De fire elementer, der udgør bagepulverAf Kylene Arnold Opdateret 24. marts 2022 Geografisk/iStock/GettyImages Bagepulver, videnskabeligt kendt som natriumbicarbonat, er en alsidig basisvare i husholdningen. I modsætning til bagepulver
De fire elementer, der udgør bagepulverAf Kylene Arnold Opdateret 24. marts 2022 Geografisk/iStock/GettyImages Bagepulver, videnskabeligt kendt som natriumbicarbonat, er en alsidig basisvare i husholdningen. I modsætning til bagepulver -
 Nye fremskridt for at reducere defekter i multimaterialer ved hjælp af rettet energiaflejringIfølge undersøgelsen kan manipulation af gradientforholdet mellem komponentmaterialerne under rettet energiaflejring (en 3D-printteknik) føre til højtydende funktionelle materialer med minimale defekt
Nye fremskridt for at reducere defekter i multimaterialer ved hjælp af rettet energiaflejringIfølge undersøgelsen kan manipulation af gradientforholdet mellem komponentmaterialerne under rettet energiaflejring (en 3D-printteknik) føre til højtydende funktionelle materialer med minimale defekt
- Hvordan beregnes vægten af Expandable Polystyrene Thermocol, hvis densitet er angivet?
- Ny leveringsmetode tillader langsom frigivelse af en bredere vifte af peptidlægemidler i kroppen
- Hvad kaldes det, når alle atomer er de samme?
- Hvad kan forklare, hvorfor solen er en enkelt stjerne?
- Big Basin Redwoods park genopbygger langsomt efter brande, står over for et massivt job
- En koloni af røde bakterier får lov til at gengive sig for 16 generationer, som videnskabsmand und…


