Hydrogenchlorid (HCl):Kovalent karakter forklaret
Her er hvorfor:
* Elektronegativitet: Klor er meget mere elektronegativt end brint. Dette betyder, at klor har et stærkere træk på de delte elektroner i bindingen. Selvom bindingen ikke er helt ens, er det ikke en fuld overførsel af elektroner som i en ionbinding.
* Polær kovalent: Den ulige deling af elektroner skaber en delvis positiv ladning på brint (δ+) og en delvis negativ ladning på klor (δ-). Dette gør HCl til et polært kovalent molekyle.
* Gasformig tilstand: Ved stuetemperatur er HCl en gas, som er typisk for kovalente forbindelser. Ioniske forbindelser på den anden side danner normalt faste krystaller ved stuetemperatur.
Opsummering, mens HCl udviser en vis ionisk karakter på grund af elektronegativitetsforskellen, er det primært klassificeret som en kovalent forbindelse på grund af deling af elektroner og dens gasformige tilstand.
Sidste artikelSilicium:egenskaber og hvorfor det er et rent stof
Næste artikelIoniske vs. kovalente forbindelser:Nøgleforskelle forklaret
 Varme artikler
Varme artikler
-
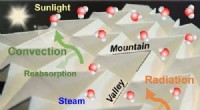 Origami inspirerer til en højeffektiv solar dampgeneratorKredit:American Chemical Society Vand dækker det meste af kloden, men mange regioner lider stadig under mangel på rent drikkevand. Hvis forskerne effektivt og bæredygtigt kunne forvandle havvand t
Origami inspirerer til en højeffektiv solar dampgeneratorKredit:American Chemical Society Vand dækker det meste af kloden, men mange regioner lider stadig under mangel på rent drikkevand. Hvis forskerne effektivt og bæredygtigt kunne forvandle havvand t -
 Ny NIST-forskning kan nedbringe omkostningerne ved at lave nikkelNår du designer en ny mønt, Amerikanske regeringsorganer som NIST bruger et dummy-aftryk for ikke at løbe på kant med reglerne mod varemærkeforfalskning. Her, Martha Washington i en pøbelkasket træder
Ny NIST-forskning kan nedbringe omkostningerne ved at lave nikkelNår du designer en ny mønt, Amerikanske regeringsorganer som NIST bruger et dummy-aftryk for ikke at løbe på kant med reglerne mod varemærkeforfalskning. Her, Martha Washington i en pøbelkasket træder -
 Planteforskere undersøger brødaroma:Moderne og gamle hvedesorter smager lige godtIdentiske opskrifter blev brugt til at bage brød fra forskellige hvedesorter, som derefter blev prøvet. Allerede det ydre udseende af hvert af brødene varierer betydeligt. Kredit:BeckaBeck Hvede e
Planteforskere undersøger brødaroma:Moderne og gamle hvedesorter smager lige godtIdentiske opskrifter blev brugt til at bage brød fra forskellige hvedesorter, som derefter blev prøvet. Allerede det ydre udseende af hvert af brødene varierer betydeligt. Kredit:BeckaBeck Hvede e -
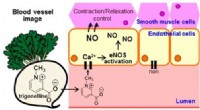 Forbindelser i monsterræddike kunne hjælpe med at tæmme hjerte-kar-sygdommeKredit:American Chemical Society Træd gulerødder til side, løg og broccoli. Den nyeste hjertesunde grøntsag kunne være en gigantisk, rekordsættende radise. I en undersøgelse, der vises i ACS Tids
Forbindelser i monsterræddike kunne hjælpe med at tæmme hjerte-kar-sygdommeKredit:American Chemical Society Træd gulerødder til side, løg og broccoli. Den nyeste hjertesunde grøntsag kunne være en gigantisk, rekordsættende radise. I en undersøgelse, der vises i ACS Tids
- Sydafrikas bevaringsmodel:Hvorfor det er en god idé at udvide brugen af biodiversitet til at gene…
- Hvad er produktionen inden for videnskab?
- Dannelse af sur regn:Hvordan svovl- og nitrogenoxider reagerer med vand
- Ny teknologi kan gøre protetiske hænder nemmere for patienter at bruge
- Californien ræser om at forudsige, hvilken by der kan blive ved med at brænde
- FAA udsat til Boeing på vigtige 737 MAX-vurderinger:kilde


