Kobber(II)sulfat (CuSO₄):Syre eller base? Forstå dens egenskaber
* Salt af en stærk syre og svag base: Kobber(II)sulfat er et salt dannet ved reaktion af en stærk syre (svovlsyre, H2SO4) og en svag base (kobberhydroxid, Cu(OH)2).
* Hydrolyse: Når CuSO4 opløses i vand, gennemgår det hydrolyse, hvilket betyder, at ionerne reagerer med vandmolekyler. Sulfat-ionen (SO₄²⁻) reagerer ikke signifikant med vand, men kobber(II)-ionen (Cu²⁺) gør det. Kobber(II)-ionen reagerer med vand og danner hydroniumioner (H₃O⁺), hvilket gør opløsningen let sur.
* pH: pH-værdien af en CuSO4-opløsning vil være lidt mindre end 7, hvilket indikerer en mild surhedsgrad.
Opsummering:
* CuSO4 er ikke en stærk syre eller en stærk base.
* Det udviser en mild surhed på grund af hydrolysen af kobber(II)-ionen.
Det er dog vigtigt at huske, at surhedsgraden af en CuSO4-opløsning kan påvirkes af faktorer som koncentration og tilstedeværelsen af andre kemikalier.
 Varme artikler
Varme artikler
-
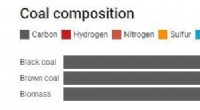 Hvordan laver vi brint af kul, og er det virkelig et rent brændstof?Kredit:Samtalen Energigiganten AGL afslørede i denne uge planer om at producere brintkraft på deres Loy Yang A-kulstation. Men hvordan forvandler vi kul, som ofte opfattes som blot lavet af kulsto
Hvordan laver vi brint af kul, og er det virkelig et rent brændstof?Kredit:Samtalen Energigiganten AGL afslørede i denne uge planer om at producere brintkraft på deres Loy Yang A-kulstation. Men hvordan forvandler vi kul, som ofte opfattes som blot lavet af kulsto -
 Denne hydrogeltablet kan rense en liter flodvand på en timeBrug af hydrogel-tabletten til at rense vand kræver ingen energitilførsel og skaber ikke skadelige biprodukter. Kredit:University of Texas i Austin. Så meget som en tredjedel af verdens befolkning
Denne hydrogeltablet kan rense en liter flodvand på en timeBrug af hydrogel-tabletten til at rense vand kræver ingen energitilførsel og skaber ikke skadelige biprodukter. Kredit:University of Texas i Austin. Så meget som en tredjedel af verdens befolkning -
 Omdannelse af fibriller til krystallerTændstik-lignende amyloidkrystaller kunne repræsentere den mest stabile foldede struktur af et protein eller en lang peptidsekvens. Kredit:Reynolds et al., Nat. Comm. 2017 Et internationalt team a
Omdannelse af fibriller til krystallerTændstik-lignende amyloidkrystaller kunne repræsentere den mest stabile foldede struktur af et protein eller en lang peptidsekvens. Kredit:Reynolds et al., Nat. Comm. 2017 Et internationalt team a -
 Stabilisering af emulsionsforskning forbedrer brandslukningsoperationer og mereKredit:Unsplash/CC0 Public Domain Forskere ved Texas A&M University har fundet en måde at kontrollere ladningen af nanopartikler på en to-væske grænseflade for at skabe et mere stabilt system, hv
Stabilisering af emulsionsforskning forbedrer brandslukningsoperationer og mereKredit:Unsplash/CC0 Public Domain Forskere ved Texas A&M University har fundet en måde at kontrollere ladningen af nanopartikler på en to-væske grænseflade for at skabe et mere stabilt system, hv
- Billede:Instant space selfies
- Hvad er den kemiske sammensætning af tandbørste?
- Hvorfor er der sne på bjergtoppene i Alaska om sommeren?
- Hvilken type kort bruges bedst til at lokalisere landformer såsom bjerge søer og ørkener?
- Hvilken type materiale er en isolator?
- Forskere løfter sløret for en omfattende samling af rhodamin-baserede fluorescerende farvestoffer


