Smeltepunktssammenligning:NaOH vs. methanol (CH3OH) - kemi forklaret
Her er hvorfor:
* Ionisk binding vs. hydrogenbinding: NaOH er en ionisk forbindelse, hvilket betyder, at den holdes sammen af stærke elektrostatiske kræfter mellem positivt ladede natriumioner (Na+) og negativt ladede hydroxidioner (OH-). Disse ionbindinger kræver meget energi at bryde, hvilket resulterer i et højt smeltepunkt.
* Hydrogenbinding i methanol: CH3OH er en kovalent forbindelse med hydrogenbinding. Mens hydrogenbindinger er stærkere end typiske dipol-dipol-interaktioner, er de stadig svagere end ionbindinger. Hydrogenbindingen i methanol bidrager til dets relativt højere smeltepunkt sammenlignet med ikke-polære molekyler, men den er ikke så stærk som ionbindingen i NaOH.
Smeltepunkter:
* NaOH: 318 °C (590 °F)
* CH3OH: -97,6 °C (-141,7 °F)
Derfor har NaOH et betydeligt højere smeltepunkt end CH3OH på grund af dets stærkere ionbinding.
Sidste artikelIoniske forbindelser i vand:Ud over H+ og OH-
Næste artikelKloroxidationstal:Forståelse af -1 og dets rolle
 Varme artikler
Varme artikler
-
 Bekræftelse af stamtavlen for urankuber fra Nazitysklands mislykkede atomprogramRobertson med PNNLs terning, som er i et beskyttende etui. Kredit:Andrea Starr/PNNL Under Anden Verdenskrig, Nazityskland og USA var kapløb om at udvikle nuklear teknologi. Før Tyskland kunne lykk
Bekræftelse af stamtavlen for urankuber fra Nazitysklands mislykkede atomprogramRobertson med PNNLs terning, som er i et beskyttende etui. Kredit:Andrea Starr/PNNL Under Anden Verdenskrig, Nazityskland og USA var kapløb om at udvikle nuklear teknologi. Før Tyskland kunne lykk -
 At manipulere med cellulære fedtstoffer lover megetSabotage med cellulære lipidmembraner giver et stort løfte. Kredit:DTU I dag, meget af den biologi, der ligger til grund for den cellulære sammensætning af lipider, er en sort boks for videnskabsm
At manipulere med cellulære fedtstoffer lover megetSabotage med cellulære lipidmembraner giver et stort løfte. Kredit:DTU I dag, meget af den biologi, der ligger til grund for den cellulære sammensætning af lipider, er en sort boks for videnskabsm -
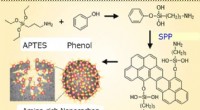 Elektrisk stød til kulstof gør en bedre vandrenserSynteseproces af nanocarbonadsorbent. Kredit:Nagahiro Saito Forskere ved Nagoya University har udviklet en et-trins fremstillingsproces, der forbedrer nanocarbons evne til at fjerne giftige tungme
Elektrisk stød til kulstof gør en bedre vandrenserSynteseproces af nanocarbonadsorbent. Kredit:Nagahiro Saito Forskere ved Nagoya University har udviklet en et-trins fremstillingsproces, der forbedrer nanocarbons evne til at fjerne giftige tungme -
 Papirbaseret teknologi fremmer tidligere opdagelse af kræftWenji Dong. Kredit:WSU Forskere fra Washington State University har udviklet en teknologi, der er mere end 30 gange mere følsom end nuværende laboratoriebaserede tests til at finde biomarkører for
Papirbaseret teknologi fremmer tidligere opdagelse af kræftWenji Dong. Kredit:WSU Forskere fra Washington State University har udviklet en teknologi, der er mere end 30 gange mere følsom end nuværende laboratoriebaserede tests til at finde biomarkører for
- Hvilken type sky dækker normalt hele himlen og bringer grå dage?
- Hvorfor eksisterer materie? Afrunding af elektroner kan indeholde spor
- Sådan beregnes RPD
- Hydrogenatomer i fosforsyre (H₃PO₄):En simpel forklaring
- En alvorlig tørke i en græsareal vil reducere antallet af forbrugere hele energipyramiden Hvorfor?…
- Tilpasning til gymnasiet:Hvorfor de fysiske rammer også er vigtige


