Ioniske forbindelser i vand:Ud over H+ og OH-
Salte:
* Natriumchlorid (NaCl): Opløses i Na+ (natriumioner) og Cl- (chloridioner).
* Kaliumnitrat (KNO3): Opløses i K+ (kaliumioner) og NO3- (nitrationer).
* Calciumcarbonat (CaCO3): Opløses let for at danne Ca2+ (calciumioner) og CO32- (carbonationer).
Syrer (bortset fra stærke syrer som HCl, HNO3, H2SO4):
* Eddikesyre (CH3COOH): Ioniserer delvist for at danne H+ (hydroniumioner) og CH3COO- (acetationer).
* Kulsyre (H2CO3): Ioniserer for at danne H+ (hydroniumioner) og HCO3- (bicarbonationer).
Baser (bortset fra stærke baser som NaOH, KOH):
* Ammoniak (NH3): Reagerer med vand og danner NH4+ (ammoniumioner) og OH- (hydroxidioner).
Andre ioniske forbindelser:
* Magnesiumsulfat (MgSO4): Opløses i Mg2+ (magnesiumioner) og SO42- (sulfationer).
* Kobber(II)chlorid (CuCl2): Opløses i Cu2+ (kobber(II)-ioner) og Cl- (chloridioner).
Vigtig bemærkning: Omfanget af ionisering afhænger af det specifikke stof og dets koncentration. Nogle stoffer er stærke elektrolytter og ioniseres fuldstændigt i vand, mens andre er svage elektrolytter og kun ioniseres delvist.
 Varme artikler
Varme artikler
-
 Forskere opdager nye og skadelige kobber-proteinkomplekserKredit:TU Delft Kobber er vigtigt for mange processer i vores krop. Det understøtter produktionen af røde blodlegemer, stofskifte, og dannelsen af bindevæv og knogler, blandt andet. Kobber er
Forskere opdager nye og skadelige kobber-proteinkomplekserKredit:TU Delft Kobber er vigtigt for mange processer i vores krop. Det understøtter produktionen af røde blodlegemer, stofskifte, og dannelsen af bindevæv og knogler, blandt andet. Kobber er -
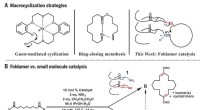 Efterligner enzymer, kemikere producerer store, nyttige carbonringeMakrocykliseringsstrategier. (A) Tidligere tilgange og foldamertilgang til makrocyklisering. (B) Divergent reaktivitet:Foldamer versus små molekyle katalyse. lign., ækvivalent(er). Kredit: Videnskab
Efterligner enzymer, kemikere producerer store, nyttige carbonringeMakrocykliseringsstrategier. (A) Tidligere tilgange og foldamertilgang til makrocyklisering. (B) Divergent reaktivitet:Foldamer versus små molekyle katalyse. lign., ækvivalent(er). Kredit: Videnskab -
 Forskere omdanner CO til CO2 med et enkelt metalatomTufts University-forsker Charles Sykes har for første gang demonstreret, at et enkelt metalatom kan fungere som en katalysator ved omdannelse af kulilte til kuldioxid. en kemisk reaktion, der almindel
Forskere omdanner CO til CO2 med et enkelt metalatomTufts University-forsker Charles Sykes har for første gang demonstreret, at et enkelt metalatom kan fungere som en katalysator ved omdannelse af kulilte til kuldioxid. en kemisk reaktion, der almindel -
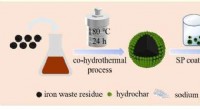 Forskere bruger tobaksaffaldsvæske og jernrester til fjernelse af Cd(II)Skematisk diagram af fremstillingsprocessen og adsorptionsmekanismerne for OWIR@TWL@SP. Kredit:WU Qingchuan Ifølge en ny undersøgelse offentliggjort i Langmuir , blev en slags jernbaseret kulstofmi
Forskere bruger tobaksaffaldsvæske og jernrester til fjernelse af Cd(II)Skematisk diagram af fremstillingsprocessen og adsorptionsmekanismerne for OWIR@TWL@SP. Kredit:WU Qingchuan Ifølge en ny undersøgelse offentliggjort i Langmuir , blev en slags jernbaseret kulstofmi
- Hvad kræver mere energismelning eller kogning?
- Hvad er produkterne fra en reaktion 6H20 plus 6C02 C6H1206 602?
- Billede:Beringstrædet
- Den mest detaljerede undersøgelse til dato af tarmindholdet i Tollundmanden
- Når tyngdekraften får en enorm mængde sten eller jord til at blive ført ned ad en hældning, kal…
- Projekt til at indsamle detaljerede data om mikroplastik starter med Stillehavets ekspedition


