Neutraliseringsreaktioner i kemi:definition, proces og eksempler
Neutralization in Chemistry:A Balancing Act
Neutralisering i kemi refererer til reaktionen mellem en syre og en base , hvilket resulterer i dannelsen af salt og vand . Denne reaktion er ofte ledsaget af frigivelse af varme, hvilket gør det til en exoterm reaktion .
Her er en oversigt:
* Syre: Et stof, der donerer hydrogenioner (H+) i opløsning. Eksempler omfatter saltsyre (HCl) og svovlsyre (H2SO4).
* Base: Et stof, der accepterer hydrogenioner (H+) i opløsning. Eksempler omfatter natriumhydroxid (NaOH) og kaliumhydroxid (KOH).
* Salt: En ionforbindelse dannet ved reaktion mellem en syre og en base. Salte kan være neutrale, sure eller basiske afhængigt af styrken af den involverede syre og base.
* Vand: Dannet af kombinationen af hydrogenioner (H+) fra syren og hydroxidioner (OH-) fra basen.
Ligningen:
Den generelle ligning for neutralisering er:
Syre + Base → Salt + Vand
Eksempel:
Neutraliseringsreaktionen mellem saltsyre (HCl) og natriumhydroxid (NaOH) producerer natriumchlorid (NaCl) og vand (H2O).
HCl (syre) + NaOH (base) → NaCl (salt) + H2O (vand)
Vigtigt:
Neutraliseringsreaktioner er afgørende i forskellige applikationer, herunder:
* pH-kontrol: Neutralisering bruges til at justere pH i opløsninger, såsom i spildevandsbehandling og industrielle processer.
* Oprydning af syrespild: Neutraliseringsmidler bruges til at neutralisere syrespild og forhindre skade på mennesker og miljø.
* Titrering: Neutraliseringsreaktioner bruges i titrering til at bestemme koncentrationen af en ukendt syre eller base.
* Medicin: Antacida, som neutraliserer mavesyre, er et almindeligt eksempel på neutralisering i medicin.
Nøglebegreber:
* pH: Et mål for surhedsgrad eller alkalinitet, hvor en pH-værdi på 7 er neutral.
* Stærk syre/base: En syre eller base, der dissocierer fuldstændigt i opløsning og frigiver alle dens H+ eller OH- ioner.
* Svag syre/base: En syre eller base, der kun delvist dissocierer i opløsning og frigiver kun nogle af dens H+ eller OH-ioner.
* Neutraliseringspunkt: Punktet i en titrering, hvor syren og basen er fuldstændig neutraliseret, hvilket resulterer i en neutral pH på 7.
Neutralisering er et grundlæggende begreb i kemi, der hjælper med at forklare opførselen af syrer og baser og deres interaktioner. Forståelse af neutraliseringsreaktioner er afgørende for forskellige videnskabelige og praktiske anvendelser.
Sidste artikelBedste materialer til saltsyretanke:Tantal og mere
Næste artikelForstå opløseligheden af bordsalt (NaCl)
 Varme artikler
Varme artikler
-
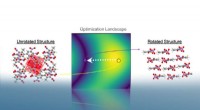 Molekylære krystalstrukturer pakker det indAutopack roterer krystalstrukturer i 3D-rum for at minimere deres molekylers projicerede areal. Efter konvergens, det er muligt at udtrække krystallens tilhørende pakningsmotiv baseret på relative int
Molekylære krystalstrukturer pakker det indAutopack roterer krystalstrukturer i 3D-rum for at minimere deres molekylers projicerede areal. Efter konvergens, det er muligt at udtrække krystallens tilhørende pakningsmotiv baseret på relative int -
 Forudsigelse af endelig temperatur i et kalorimeter:En trin-for-trin guideAf John Brennan, Opdateret 24. marts 2022 Billedkredit:tonuacatic/iStock/GettyImages Kalorimetri er en hjørnesten i eksperimentel termokemi, som gør det muligt for forskere at bestemme reaktionsenta
Forudsigelse af endelig temperatur i et kalorimeter:En trin-for-trin guideAf John Brennan, Opdateret 24. marts 2022 Billedkredit:tonuacatic/iStock/GettyImages Kalorimetri er en hjørnesten i eksperimentel termokemi, som gør det muligt for forskere at bestemme reaktionsenta -
 Videnskaben bag perfekte kartofler:Undgå klistret tekstur med præcisionJag_cz/Getty Images Vi modtager muligvis en kommission på køb foretaget fra links. Kartofler kan være en vidunderlig, solid akkompagnement til mange retter - men kun hvis de tilberedes korrekt. Over
Videnskaben bag perfekte kartofler:Undgå klistret tekstur med præcisionJag_cz/Getty Images Vi modtager muligvis en kommission på køb foretaget fra links. Kartofler kan være en vidunderlig, solid akkompagnement til mange retter - men kun hvis de tilberedes korrekt. Over -
 Sådan laver du en 1:4-fortynding:Bland en del koncentrat med fire dele vandAf Melissa Mayer Opdateret 30. august 2022 Irina Vodneva/iStock/GettyImages Fra husholdningsrengøringsmidler til laboratorieprøver er simple fortyndinger overalt. At mestre fortyndingsforhold giver
Sådan laver du en 1:4-fortynding:Bland en del koncentrat med fire dele vandAf Melissa Mayer Opdateret 30. august 2022 Irina Vodneva/iStock/GettyImages Fra husholdningsrengøringsmidler til laboratorieprøver er simple fortyndinger overalt. At mestre fortyndingsforhold giver
- Hvordan adskiller videnskabsmænd i hellenistiske tider sig fra forskere tid i deres tænkning på j…
- Natriumbicarbonat:Fysiske og kemiske egenskaber forklaret
- Hvor mange joules er der behov for for at smelte 2 gram vand?
- Bilbies kunne hoppe tilbage i milde klimazoner, viser undersøgelse
- Hvilken slags energi kaldes også termisk energi?
- Ændret bakteriel adfærd i rummet kan skyldes reduceret ekstracellulær transport


