Vands opløsningsevne:Forståelse af ioniske forbindelser
1. Polar natur:
* Vandmolekyler har en bøjet form med ilt i toppunktet og to brintatomer i bunden.
* Ilt er mere elektronegativt end brint, hvilket betyder, at det tiltrækker elektroner stærkere. Dette skaber en delvis negativ ladning (δ-) på oxygenatomet og en delvis positiv ladning (δ+) på hydrogenatomerne.
* Denne ulige fordeling af ladning gør vand til et polært molekyle, hvilket betyder, at det har en positiv og en negativ ende.
2. Hydrogenbinding:
* De delvise positive ladninger på brintatomerne i et vandmolekyle kan danne svage elektrostatiske attraktioner, kaldet hydrogenbindinger, med de delvise negative ladninger på iltatomerne i andre vandmolekyler.
* Disse brintbindinger skaber et sammenhængende netværk af vandmolekyler.
3. Opløsning af ioniske stoffer:
* Når en ionforbindelse (som salt, NaCl) anbringes i vand, omgiver de polære vandmolekyler ionerne.
* De negativt ladede iltatomer i vandmolekyler tiltrækkes af de positivt ladede natriumioner (Na+).
* På samme måde tiltrækkes de positivt ladede brintatomer i vandmolekyler af de negativt ladede chloridioner (Cl-).
* Disse attraktioner overvinder de elektrostatiske kræfter, der holder ionerne sammen i det faste krystalgitter.
* Ionerne er derefter omgivet af vandmolekyler, bliver hydreret og bevæger sig frit i opløsning, hvilket effektivt opløser den ioniske forbindelse.
Opsummering:
* Vands polære natur gør det muligt at tiltrække og omgive ioner og adskille dem fra hinanden.
* Hydrogenbindingsnetværket i vand hjælper med at stabilisere de opløste ioner.
Dette forklarer, hvorfor vand er et fremragende opløsningsmiddel for mange ioniske stoffer, hvilket fører til dets vigtige roller i biologiske systemer, kemiske reaktioner og andre anvendelser.
Sidste artikelForståelse af ilts delvise negative ladning i vandmolekyler
Næste artikelForstå bagepulver:Sådan fungerer det som hævemiddel
 Varme artikler
Varme artikler
-
 Neurotransmittere på et øjeblikForskning udført på IPC PAS ved hjælp af den nye forskningsmetode muliggør tidlig påvisning af neurotransmittermangler, som hjælper med at forhindre forskellige sygdomme. På billedet ses Magdalena Kun
Neurotransmittere på et øjeblikForskning udført på IPC PAS ved hjælp af den nye forskningsmetode muliggør tidlig påvisning af neurotransmittermangler, som hjælper med at forhindre forskellige sygdomme. På billedet ses Magdalena Kun -
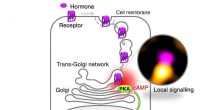 Hvordan receptorer for medicin virker inde i cellerNyopdaget mekanisme for GPCR-signalering ved trans-Golgi-netværket (TGN). Ved binding af et hormon (TSH), receptoren optages af cellen (internalisering) og transporteres til TGN, hvor det inducerer lo
Hvordan receptorer for medicin virker inde i cellerNyopdaget mekanisme for GPCR-signalering ved trans-Golgi-netværket (TGN). Ved binding af et hormon (TSH), receptoren optages af cellen (internalisering) og transporteres til TGN, hvor det inducerer lo -
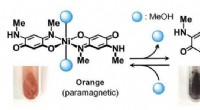 Ny type sensormateriale udvikletNikkel(II)-quinonoidkomplekser skifter deres farver og magnetisme ved at absorbere eller frigive methanol. Kredit:Hokkaido University Forskere fra Hokkaido University er lykkedes med at udvikle et
Ny type sensormateriale udvikletNikkel(II)-quinonoidkomplekser skifter deres farver og magnetisme ved at absorbere eller frigive methanol. Kredit:Hokkaido University Forskere fra Hokkaido University er lykkedes med at udvikle et -
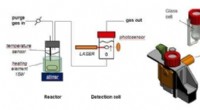 Ny simpel enhed forbedrer analysen af reaktionskinetikken i høj gradBobletællerenheden. Fra venstre til højre:skematisk fremstilling af reaktionskammeret og detektionscellen; ortografisk projektion af detektionscellen og dens hus; og billede af systemet i en praktisk
Ny simpel enhed forbedrer analysen af reaktionskinetikken i høj gradBobletællerenheden. Fra venstre til højre:skematisk fremstilling af reaktionskammeret og detektionscellen; ortografisk projektion af detektionscellen og dens hus; og billede af systemet i en praktisk


