Reversible kemiske reaktioner:Forståelse af ligevægt og processer
Reversible reaktioner:
* Definition: En reversibel reaktion er en kemisk reaktion, der kan forløbe i både fremadgående og bagudgående retning. Det betyder, at produkterne kan reagere og danne de oprindelige reaktanter igen.
* Ligevægt: Reversible reaktioner når en tilstand af ligevægt, hvor hastighederne for de fremadrettede og omvendte reaktioner er ens. Dette betyder, at koncentrationerne af reaktanter og produkter forbliver konstante over tid.
* Betingelser for reversibilitet: Mange faktorer kan påvirke, om en reaktion er reversibel, herunder:
* Temperatur: Stigende temperatur kan begunstige den endoterme retning af en reaktion.
* Tryk: Ændring af tryk kan favorisere den side af reaktionen med færre mol gas.
* Koncentration: Tilføjelse af flere reaktanter eller produkter kan flytte ligevægten for at favorisere den modsatte retning.
Eksempler på reversible kemiske ændringer:
* Vand: Reaktionen mellem brint og ilt for at danne vand er reversibel.
* 2H2(g) + O2(g) ⇌ 2H2O(l)
* Kulsyre: Reaktionen mellem kuldioxid og vand til dannelse af kulsyre er reversibel.
* CO₂(g) + H₂O(l) ⇌ H₂CO3(aq)
* Nitrogendioxid: Dimeriseringen af nitrogendioxid er en reversibel reaktion.
* 2NO₂(g) ⇌ N₂O₄(g)
Vigtige bemærkninger:
* Ikke alle kemiske ændringer er reversible. Mange reaktioner er irreversible, hvilket betyder, at de kun går i én retning. For eksempel er afbrænding af træ en kemisk forandring, som ikke let kan vendes.
* Omfanget af reversibilitet kan variere. Nogle reaktioner er mere reversible end andre, afhængigt af betingelserne og arten af reaktanterne og produkterne.
Lad mig vide, hvis du gerne vil udforske specifikke eksempler eller dykke dybere ned i begrebet ligevægt!
 Varme artikler
Varme artikler
-
 Bekæmpelse af et mægtigt ukrudtKredit:CC0 Public Domain Ukrudt er irriterende i enhver situation. Nu, forestil dig et ukrudt, der er så besværligt, at det har muteret til at modstå flere herbicider. Palmer amaranth, et medlem a
Bekæmpelse af et mægtigt ukrudtKredit:CC0 Public Domain Ukrudt er irriterende i enhver situation. Nu, forestil dig et ukrudt, der er så besværligt, at det har muteret til at modstå flere herbicider. Palmer amaranth, et medlem a -
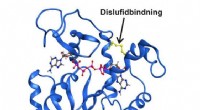 At få øje på det usynligeHøjopløsningsrøntgenstruktur af enzymet adenylatkinase fanget i en forbigående strukturel tilstand af en kovalent disulfidbinding. Kredit:Umeå Universitet Det er lykkedes kemikere ved Umeå Univers
At få øje på det usynligeHøjopløsningsrøntgenstruktur af enzymet adenylatkinase fanget i en forbigående strukturel tilstand af en kovalent disulfidbinding. Kredit:Umeå Universitet Det er lykkedes kemikere ved Umeå Univers -
 Udskrivning af plastikbaner for at beskytte fremtidens mobiltelefonskærmePolycarbonatbaner syntetiseret ved hjælp af additiv fremstilling absorberer op til 96% af slagenergien. Kredit:Shibo Zou Følg den ubrydelige hoppende telefon! Et team fra Polytechnique Montréal de
Udskrivning af plastikbaner for at beskytte fremtidens mobiltelefonskærmePolycarbonatbaner syntetiseret ved hjælp af additiv fremstilling absorberer op til 96% af slagenergien. Kredit:Shibo Zou Følg den ubrydelige hoppende telefon! Et team fra Polytechnique Montréal de -
 Infrarød sensor fungerer som et nyt værktøj til opdagelse af lægemidlerKredit:Sisacom, Shutterstock Forskere har fundet en ny metode til at analysere, hvordan aktive midler påvirker et specifikt protein, der er vigtigt for celleoverlevelse. Deres forskning kan hjælpe
Infrarød sensor fungerer som et nyt værktøj til opdagelse af lægemidlerKredit:Sisacom, Shutterstock Forskere har fundet en ny metode til at analysere, hvordan aktive midler påvirker et specifikt protein, der er vigtigt for celleoverlevelse. Deres forskning kan hjælpe


