Elektronkonfiguration og oktetreglen:Magnesium som eksempel
Magnesiums elektronkonfiguration:
* Magnesium har et atomnummer på 12, hvilket betyder, at det har 12 protoner og 12 elektroner.
* Dens elektronkonfiguration er 1s² 2s² 2p⁶ 3s².
* Det betyder, at dets yderste energiniveau (det 3. energiniveau) kun har 2 elektroner i 3s orbitalen.
Oktetreglen:
* Oktetreglen siger, at atomer har tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration med 8 elektroner i deres yderste energiniveau (valensskal).
* Denne stabile konfiguration ligner ædelgasserne, som er meget ureaktive.
Magnesiums løsning:
* Magnesium har kun 2 valenselektroner, så det skal vinde 6 mere for at opnå en oktet.
* Det er dog nemmere for magnesium at tabe dens 2 valenselektroner for at opnå den stabile konfiguration af den tidligere ædelgas (neon, med 10 elektroner, 2 i 1. skal og 8 i 2.).
* Ved at miste disse elektroner bliver magnesium til en positivt ladet ion (Mg²⁺) med en fuld ydre skal på 8 elektroner fra det tidligere energiniveau.
Danning af en ionisk binding:
* Magnesium kan så danne en ionbinding med et grundstof som klor (Cl), som har 7 valenselektroner.
* Klor skal få 1 elektron for at fuldføre sin oktet og bliver til en negativt ladet ion (Cl⁻).
* Den elektrostatiske tiltrækning mellem den positivt ladede magnesiumion (Mg²⁺) og den negativt ladede chlorion (Cl⁻) danner en ionbinding, hvilket resulterer i forbindelsen magnesiumchlorid (MgCl₂).
Sammenfattende opnår magnesium en fuld ydre skal ved at miste sine 2 valenselektroner og blive en positivt ladet ion. Dette gør det muligt for den at danne en ionbinding med andre atomer for at opnå stabilitet.
Sidste artikelChloridion:Forståelse af negativt ladede kloratomer
Næste artikelSvovlsmeltepunkt:Egenskaber og allotroper
 Varme artikler
Varme artikler
-
 CRISPR udvinder bakteriegenom til skjulte farmaceutiske skatteIllinois-forskere brugte CRISPR-teknologi til at aktivere tavse genklynger i Streptomyces bakterie, en potentiel skatkammer af nye klasser af stoffer. Afbildet, med uret bagfra i midten:kandidatstud
CRISPR udvinder bakteriegenom til skjulte farmaceutiske skatteIllinois-forskere brugte CRISPR-teknologi til at aktivere tavse genklynger i Streptomyces bakterie, en potentiel skatkammer af nye klasser af stoffer. Afbildet, med uret bagfra i midten:kandidatstud -
 Ny test giver nøjagtige mål for DNA-skader fra kemiske forbindelserKredit:CC0 Public Domain En ny biomarkørtest udviklet af forskere ved Georgetown Lombardi Comprehensive Cancer Center og deres kolleger kan hjælpe med at forudsige, med op til 90 procent sikkerhed
Ny test giver nøjagtige mål for DNA-skader fra kemiske forbindelserKredit:CC0 Public Domain En ny biomarkørtest udviklet af forskere ved Georgetown Lombardi Comprehensive Cancer Center og deres kolleger kan hjælpe med at forudsige, med op til 90 procent sikkerhed -
 Gedemælkskefir har vist sig at være godt for dit helbredKredit:CC0 Public Domain Kefir er et fermenteret mejeriprodukt, der gradvist bliver mere og mere almindeligt på hylderne i spanske butikker og supermarkeder. Da det er et mælkebaseret produkt, fre
Gedemælkskefir har vist sig at være godt for dit helbredKredit:CC0 Public Domain Kefir er et fermenteret mejeriprodukt, der gradvist bliver mere og mere almindeligt på hylderne i spanske butikker og supermarkeder. Da det er et mælkebaseret produkt, fre -
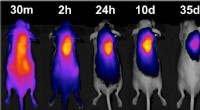 Et hyppelys for kemoterapilægemidlerHos mus, en hydrogel rekrutterer et farvestoffemærket molekyle (farvede områder) til sin placering, viser dets potentiale til at være et hjemfyrtårn for kræftmedicin. Kredit:Tilpasset fra ACS Central
Et hyppelys for kemoterapilægemidlerHos mus, en hydrogel rekrutterer et farvestoffemærket molekyle (farvede områder) til sin placering, viser dets potentiale til at være et hjemfyrtårn for kræftmedicin. Kredit:Tilpasset fra ACS Central
- Gravitationskræfter i protoplanetariske skiver kan skubbe superjorden tæt på deres stjerner
- Kan forsikringspræmier sikre, at vi kommer igennem klimaforandringerne i ét stykke?
- Hvilken har den højeste energneutron eller foton?
- Hvad er absolut nulpunkt?
- Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddel
- Hvad er når et livløst objekt givet menneskelige kvalitter?


