Forudsigelse af metaludskiftning i forbindelser:Brug af aktivitetsserien
Sådan fungerer det:
1. Aktivitetsserien: Aktivitetsserien er en liste over metaller arrangeret i rækkefølge efter deres faldende reaktivitet. De mest reaktive metaller er i toppen, og de mindst reaktive er i bunden.
2. Forudsigelse af udskiftning:
* Et metal højere på aktivitetsserien vil fortrænge (erstatte) et metal lavere på serien fra dets forbindelse.
* Et metal lavere på aktivitetsserien vil *ikke* fortrænge et metal højere på serien fra dets forbindelse.
Eksempel:
Lad os overveje reaktionen af zink (Zn) med kobbersulfat (CuSO4):
* Zn er højere på aktivitetsserien end Cu .
* Det betyder, at zink er mere reaktivt end kobber.
* Zink erstatter kobber i forbindelsen, danner zinksulfat (ZnSO4) og efterlader elementært kobber.
Reaktion: Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s)
Nøglepunkter:
* Metaller over brint kan fortrænge brint fra syrer.
* Metaller under brint kan ikke fortrænge brint fra syrer.
* Aktivitetsserien er en generel retningslinje, og der kan være undtagelser baseret på specifikke reaktionsforhold.
Her er en enkel måde at huske aktivitetsserien på:
* Kalium (K), Natrium (Na), Lithium (Li) :De mest reaktive metaller
* Calcium (Ca), Magnesium (Mg), Aluminium (Al), Zink (Zn), Jern (Fe), Tin (Sn), Bly (Pb), Hydrogen (H), Kobber (Cu), Sølv (Ag), Guld (Au), Platin (Pt): Mindre reaktive metaller i faldende rækkefølge.
Husk: Du kan finde en mere komplet og præcis aktivitetsserie i din lærebog i kemi eller onlineressourcer.
 Varme artikler
Varme artikler
-
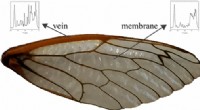 Hvordan cikader formår at vinge denKredit:American Chemical Society I modsætning til græshopper og mange andre flyvende insekter, Cikader svæver ikke gennem luften med den største lethed. Nu i en undersøgelse, der viser ACS Journa
Hvordan cikader formår at vinge denKredit:American Chemical Society I modsætning til græshopper og mange andre flyvende insekter, Cikader svæver ikke gennem luften med den største lethed. Nu i en undersøgelse, der viser ACS Journa -
 Sådan fremstilles kaliumhydroxid:metoder, kemi og sikkerhedAf Vincent Summers, Opdateret 24. marts 2022 Kaliumhydroxid (KOH) er en stærk base afledt af alkalimetalkalium (atomnummer 19). Det er et nøgleudgangsmateriale til syntesen af de fleste kaliumsalte o
Sådan fremstilles kaliumhydroxid:metoder, kemi og sikkerhedAf Vincent Summers, Opdateret 24. marts 2022 Kaliumhydroxid (KOH) er en stærk base afledt af alkalimetalkalium (atomnummer 19). Det er et nøgleudgangsmateriale til syntesen af de fleste kaliumsalte o -
 Biologi og kemi kombineres for at generere nye antibiotikaFrugtlegemer fra svampen Clitopilus passeckerianus genereret i laboratoriet. Kredit:University of Bristol Kombinerer innovationerne inden for syntetisk biologi med biologi og kemi, et team af vi
Biologi og kemi kombineres for at generere nye antibiotikaFrugtlegemer fra svampen Clitopilus passeckerianus genereret i laboratoriet. Kredit:University of Bristol Kombinerer innovationerne inden for syntetisk biologi med biologi og kemi, et team af vi -
 Vandflasker, andre genbrugte 3-D-printmaterialer kunne undgå forsyningsproblemer fra militæretMed 3D-printere, soldater kunne snart bruge genbrugsflasker og andre affaldsmaterialer til at lave vitale dele, såsom dette bilradiobeslag. Kredit:Nicole Zander/U.S. Hærens forskningslaboratorium
Vandflasker, andre genbrugte 3-D-printmaterialer kunne undgå forsyningsproblemer fra militæretMed 3D-printere, soldater kunne snart bruge genbrugsflasker og andre affaldsmaterialer til at lave vitale dele, såsom dette bilradiobeslag. Kredit:Nicole Zander/U.S. Hærens forskningslaboratorium


