Sådan fremstilles kaliumhydroxid:metoder, kemi og sikkerhed
Af Vincent Summers, Opdateret 24. marts 2022
Kaliumhydroxid (KOH) er en stærk base afledt af alkalimetalkalium (atomnummer 19). Det er et nøgleudgangsmateriale til syntesen af de fleste kaliumsalte og har udbredte industrielle og laboratoriemæssige anvendelser.
Trin 1:Fra metallisk kalium
Selvom det ikke er kommercielt levedygtigt på grund af sikkerhedsproblemer, reagerer kaliummetal voldsomt med vand for at producere KOH og brintgas:
2K + 2H2 O → 2 KOH + H2
Reaktionen frigiver en stor mængde varme, smelter metallet og får den frigjorte brint til at antændes med en karakteristisk lilla flamme. Selv et stykke kalium på størrelse med en ærte kan udløse denne eksplosive adfærd.
Trin 2:Fra træaske
Tidlige bosættere ekstraherede kaliumcarbonat fra træaske, som kan omdannes til KOH ved opvarmning og efterfølgende hydrering:
K2 CO3 → K2 O + CO2 (høj temperatur)
K2 O + H2 O → 2 KOH
Brug en ovn til at nå temperaturer over 700°C for at drive nedbrydningen af K2 CO3 .
Trin 3:Elektrolyse af kaliumchloridopløsning
Elektrolysering af en vandig KCl-opløsning producerer klorgas ved anoden og KOH ved katoden:
2 KCl + 2 H2 O → 2 KOH + Cl2 + H2
Saml klorgassen sikkert eller udluft den til atmosfæren, og høst KOH fra elektrolytten.
Trin 4:Fra andre kaliumforbindelser
Kaliumhydroxid kan også udvindes af forskellige kaliumsalte, selvom disse veje typisk er upraktiske til produktion i stor skala. For eksempel reagerer kaliumazid med vand for at give KOH, ammoniak og varme:
2 K3 N + 6 H2 O → 6 KOH + 2 NH3 + …
På samme måde producerer kaliumacetylid og kaliumhydrid KOH sammen med henholdsvis acetylen og hydrogengas.
Ting påkrævet
- Reagenser (kaliummetal, træaske, KCl osv.)
- Ovn eller højtemperaturovn
- Elektrolyseopsætning (elektroder, strømkilde, indeslutning)
- Relevant sikkerhedsudstyr (handsker, beskyttelsesbriller, laboratoriefrakke, stinkskab)
Advarsel
KOH er stærkt ætsende og kan forårsage alvorlige kemiske forbrændinger, luftvejsirritation og permanent øjenskade. Se altid sikkerhedsdatabladet (MSDS) før håndtering. Brug kun uddannet personale, og brug fuld øjenbeskyttelse, kemikalieresistente handsker og ansigtsskærm eller beskyttelsesbriller. Udfør reaktioner i et godt ventileret område eller under et stinkskab for at undgå indånding af giftige gasser.
 Varme artikler
Varme artikler
-
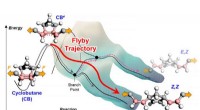 Kemiske reaktioner bryder fri fra energibarrierer ved at bruge flyby-banerEn illustration, der viser et molekyles bevægelse hen over en potentiel energioverflade på den måde, vandrere følger konturkortet over bjerge og dale langs en sti. Når der påføres en mekanisk kraft, e
Kemiske reaktioner bryder fri fra energibarrierer ved at bruge flyby-banerEn illustration, der viser et molekyles bevægelse hen over en potentiel energioverflade på den måde, vandrere følger konturkortet over bjerge og dale langs en sti. Når der påføres en mekanisk kraft, e -
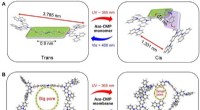 Mikroporøse polymermembraner til let-gatet iontransportSkematisk repræsentation af bottom-up designstrategien for konstruktion af kunstig lys-gatet ionkanalmembran. (A) Trans-cis-trans reversibel isomerisering af den syntetiserede azo-CMP-monomer og (B) d
Mikroporøse polymermembraner til let-gatet iontransportSkematisk repræsentation af bottom-up designstrategien for konstruktion af kunstig lys-gatet ionkanalmembran. (A) Trans-cis-trans reversibel isomerisering af den syntetiserede azo-CMP-monomer og (B) d -
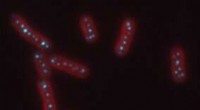 Forståelse af membranen i membranløse organellerPå billedet ses et fluorescensbillede af cyanobakterier, i rødt, med carboxysomer, i cyan. Kredit:Biteen og Vecchiarelli Labs Organeller i celler er små motorer, der indkapsler processer, der till
Forståelse af membranen i membranløse organellerPå billedet ses et fluorescensbillede af cyanobakterier, i rødt, med carboxysomer, i cyan. Kredit:Biteen og Vecchiarelli Labs Organeller i celler er små motorer, der indkapsler processer, der till -
 Denne RNA-baserede teknik kunne gøre genterapi mere effektivKredit:CC0 Public Domain Levering af funktionelle gener til celler for at erstatte muterede gener, en metode kendt som genterapi, har potentiale til behandling af mange former for sygdomme. De tid
Denne RNA-baserede teknik kunne gøre genterapi mere effektivKredit:CC0 Public Domain Levering af funktionelle gener til celler for at erstatte muterede gener, en metode kendt som genterapi, har potentiale til behandling af mange former for sygdomme. De tid
- Hvilken aminosyre findes i vandopløseligt kugleformet protein?
- Ny kvanteeffekt fundet:Spin-rotationskobling
- Er tvær- og kongresbølger en type mekanisk bølge?
- Shape-morphing mikrorobotter leverer lægemidler til kræftceller
- Menneskelig evolution:Tidslinje, stadier, teorier og beviser – en omfattende oversigt
- Er jorden større end sol?


