Forståelse af metaliondannelse:hvorfor metaller mister elektroner
* Lav ioniseringsenergi: Metaller har generelt lav ioniseringsenergi, hvilket betyder, at det kræver relativt lidt energi at fjerne en elektron fra deres yderste skal. Dette gør det energetisk gunstigt for dem at miste elektroner.
* Metallisk binding: Metaller har en unik bindingsstruktur kaldet metallisk binding. Ved denne type binding bliver metalatomernes yderste elektroner delokaliseret og danner et "hav" af elektroner, der kan bevæge sig frit gennem metalgitteret. Dette hav af elektroner er ansvarlig for den fremragende elektriske ledningsevne af metaller.
* Elektropositivitet: Metaller er elektropositive, hvilket betyder, at de har en tendens til at miste elektroner og blive positivt ladede. Dette skyldes deres tendens til at miste elektroner for at opnå en stabil elektronkonfiguration (normalt en oktet).
Her er en forenklet forklaring:
Forestil dig et metalatom med nogle få elektroner i den yderste skal. Disse elektroner er løst bundet til atomet og kan nemt fjernes. Når et metalatom mister en elektron, bliver det en positivt ladet ion, fordi det nu har flere protoner (positivt ladede partikler) end elektroner (negativt ladede partikler).
Eksempel:
Natrium (Na) har en elektron i sin yderste skal. Den mister let denne elektron for at blive en natriumion (Na+) med en +1 ladning. Den tabte elektron kan så bidrage til "havet af elektroner" i metallisk binding.
Opsummering: Metaller har en tendens til at miste elektroner og danne positive ioner på grund af deres lave ioniseringsenergier, deres metalliske bindingsstruktur og deres elektropositive natur. Dette elektrontab fører til dannelsen af stabile positive ioner og bidrager til metallers unikke egenskaber.
 Varme artikler
Varme artikler
-
 Genbrug af drivhusgasser:Nanopartikler på perovskitkrystaller undgår kokseffektFlorian Schrenk (til venstre) og Christoph Rameshan. Kredit:Vienna University of Technology Hvor som helst produktionen af skadelige drivhusgasser ikke kan forhindres, bør de omdannes til noget n
Genbrug af drivhusgasser:Nanopartikler på perovskitkrystaller undgår kokseffektFlorian Schrenk (til venstre) og Christoph Rameshan. Kredit:Vienna University of Technology Hvor som helst produktionen af skadelige drivhusgasser ikke kan forhindres, bør de omdannes til noget n -
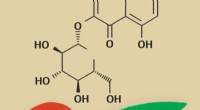 Biokemikere forbinder polyfenoler i ferskenblade med deres ekstrakts antioxidanteffektKredit:RUDN Universitet Biokemikere fra RUDN University har fastslået, hvilke stoffer i ferskenblade, der giver den antioxidante virkning af deres ekstrakt. De undersøgte sammensætningen af pulv
Biokemikere forbinder polyfenoler i ferskenblade med deres ekstrakts antioxidanteffektKredit:RUDN Universitet Biokemikere fra RUDN University har fastslået, hvilke stoffer i ferskenblade, der giver den antioxidante virkning af deres ekstrakt. De undersøgte sammensætningen af pulv -
 Natriumpolyacrylat:En alsidig superabsorberende polymerAf Natasha Gilani, opdateret 24. marts 2022. Natriumpolyacrylat, også kendt som akrylnatriumsaltpolymer, er en højtydende superabsorberende polymer, der er meget udbredt på tværs af flere industrier.
Natriumpolyacrylat:En alsidig superabsorberende polymerAf Natasha Gilani, opdateret 24. marts 2022. Natriumpolyacrylat, også kendt som akrylnatriumsaltpolymer, er en højtydende superabsorberende polymer, der er meget udbredt på tværs af flere industrier. -
 Maskinlæringssystem fremskynder opdagelsen af nye materialer til 3D-printKredit:Pixabay/CC0 Public Domain Den voksende popularitet af 3D-print til fremstilling af alle slags genstande, fra tilpasset medicinsk udstyr til billige hjem, har skabt mere efterspørgsel efter
Maskinlæringssystem fremskynder opdagelsen af nye materialer til 3D-printKredit:Pixabay/CC0 Public Domain Den voksende popularitet af 3D-print til fremstilling af alle slags genstande, fra tilpasset medicinsk udstyr til billige hjem, har skabt mere efterspørgsel efter
- Hvad er et mål for, hvor hurtigt atomer i materiale bevæger sig?
- Hvad er den kemiske formel for vandig berylliumiodid reagerer med vandig tin 2 -nitrat til dannelse …
- Hvad er betydningen af videnskab i din dag for aktivitet?
- Hvad er 58K i sten?
- De fleste jordskred i det vestlige Oregon udløst af kraftig nedbør, ikke store jordskælv
- Hvad producerer andet ilt end planter?


