Formaldehyd Carbon Hybridization:En detaljeret forklaring
1. Formaldehyds struktur
Formaldehyd har et centralt carbonatom dobbeltbundet til et oxygenatom og enkeltbundet til to hydrogenatomer. Dens Lewis-struktur ser sådan ud:
H
|
C =O
|
H
2. Hybridisering
* Carbons valenselektroner: Kulstof har fire valenselektroner (2s² 2p²)
* Hybridisering: For at danne bindingerne i formaldehyd gennemgår kulstof sp² hybridisering . Dette betyder:
* Én 2s orbitaler og to 2p orbitaler danner sammen til tre sp² hybridorbitaler . Disse hybridorbitaler er arrangeret i en trigonal plan geometri med bindingsvinkler på cirka 120°.
* Den resterende 2p orbital på kulstof forbliver uhybridiseret.
3. Obligationsdannelse
* Sigma-obligationer:
* To af sp² hybridorbitaler på carbon danner sigma (σ) bindinger med 1s orbitaler af de to hydrogenatomer.
* En af sp² hybridorbitaler på carbon danner en sigma (σ) binding med 2p orbitalen af oxygenatomet.
* Pi Bond:
* Den uhybridiserede 2p orbital på carbon overlapper med en uhybridiseret 2p orbital på oxygen for at danne en pi (π) binding. Denne pi-binding er ansvarlig for dobbeltbindingen mellem kulstof og oxygen.
4. Resumé
Sammenfattende er carbonatomet i formaldehyd sp² hybridiseret, hvilket resulterer i:
* Tre sp² hybridorbitaler: Dann sigma-bindinger med de to hydrogenatomer og oxygenatomet.
* Én uhybridiseret 2p orbital: Danner en pi-binding med oxygenatomet.
Denne hybridisering og bindingsdannelse giver formaldehyd en plan geometri med bindingsvinkler tæt på 120°.
Sidste artikelProtoner i organisk kemi:rolle, surhed og basiskhed
Næste artikelForståelse af elementer:kulstof og brint forklaret
 Varme artikler
Varme artikler
-
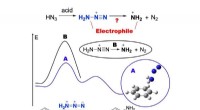 Kemikere beviser mekanismen for direkte aminering fra benzenDet grafiske abstrakt af direkte aminering. Kredit:Tomsk Polytechnic University (TPU) Et team af kemikere fra Tomsk Polytekniske Universitet opdagede en mekanisme for direkte elektrofil aminering
Kemikere beviser mekanismen for direkte aminering fra benzenDet grafiske abstrakt af direkte aminering. Kredit:Tomsk Polytechnic University (TPU) Et team af kemikere fra Tomsk Polytekniske Universitet opdagede en mekanisme for direkte elektrofil aminering -
 Sådan beregnes entalpi af reaktion nøjagtigtAf Tracy McConnell Opdateret 24. marts 2022 BZA/iStock/GettyImages Entalpi er relateret til den varme, der enten afgives ved en reaktion eller kræves for, at en reaktion kan finde sted. Det er rel
Sådan beregnes entalpi af reaktion nøjagtigtAf Tracy McConnell Opdateret 24. marts 2022 BZA/iStock/GettyImages Entalpi er relateret til den varme, der enten afgives ved en reaktion eller kræves for, at en reaktion kan finde sted. Det er rel -
 Tværfaglige interaktioner inspirerer til nye opdagelserTakayuki Kojima med det katalytiske målesystem. Kredit:Tohoku University Efter en tværfaglig tilgang, forskere i Japan har fundet nye katalysatorer ved hjælp af unikke Heusler-legeringer. De flest
Tværfaglige interaktioner inspirerer til nye opdagelserTakayuki Kojima med det katalytiske målesystem. Kredit:Tohoku University Efter en tværfaglig tilgang, forskere i Japan har fundet nye katalysatorer ved hjælp af unikke Heusler-legeringer. De flest -
 En grønnere vej til blå:Ny metode reducerer drastisk mængden af opløsningsmiddel, der er nødv…Udvikling af farvestofdannelse i løbet af 48 timers reaktionstid, efter opløsning af samme mængde faststof i samme mængde opløsningsmiddel. Kredit:Aalto University/Sandra Kaabel Phthalocyaniner bru
En grønnere vej til blå:Ny metode reducerer drastisk mængden af opløsningsmiddel, der er nødv…Udvikling af farvestofdannelse i løbet af 48 timers reaktionstid, efter opløsning af samme mængde faststof i samme mængde opløsningsmiddel. Kredit:Aalto University/Sandra Kaabel Phthalocyaniner bru


