Sådan beregnes entalpi af reaktion nøjagtigt
Af Tracy McConnell Opdateret 24. marts 2022
BZA/iStock/GettyImages
Entalpi er relateret til den varme, der enten afgives ved en reaktion eller kræves for, at en reaktion kan finde sted. Det er relateret til styrken af bindingerne i et stof, fordi der er potentiel energi i disse bindinger.
For at forstå entalpi skal først energi og termodynamik forstås. Hvad er termodynamik? Det er det kvantitative undersøgelse af energioverførsler og transformationer.
Energiformer
Energiformer
Der er mange former for energi:elektrisk energi, potentiel versus kinetisk energi, kemisk (binding) energi eller varme. Atomer eller molekyler kan have elektrisk energi i den forstand, at elektronerne kan opnås eller doneres. Elektrisk energi er ekstremt vigtig, fordi elektronernes adfærd bestemmer, hvordan et atom, et molekyle eller et stof reagerer.
Den elektriske energi af molekyler relaterer sig til begrebet stabilitet:Hvad elektroner vil gøre. Orbitaler ønsker skal udfyldes. Positive og negative ladninger tiltrækker hinanden for at opnå det lavest mulige energiniveau. Partikler med samme ladning vil afvise hinanden. Dette hjælper med at forudsige, hvad elektroner vil gøre.
Ved dannelsen af bindinger mellem atomer frigives eller kræves energi. Den mængde energi, der kræves for at binde elementer sammen, kaldes **bindingsenergi.**
Energioverførsler og -transformationer:
- Kollisioner overfører kinetisk energi fra et objekt i bevægelse til et andet objekt.
- Et varmt stof ved siden af et køligere stof vil resultere i en overførsel af energi (termisk) fra det ene til det andet.
- Potentiel energi overføres til kinetisk energi, når en sten falder fra en afsats. Når klippen rammer jorden, omdannes dens kinetiske energi til termisk energi.
- I en forbrændingsreaktion omdannes kemisk energi til termisk energi.
- I reaktioner, der ændrer molekylær sammensætning, kræves eller frigives energi.
loven om energibevarelse angiver, at energi hverken skabes eller ødelægges.
Begrebet et system og omgivelser i et lukket system er meget vigtig i termodynamik. Når man måler temperaturændringer, er det overførslen af energi fra systemet til omgivelserne (eller omvendt), man måler. Den samlede mængde energi ændres ikke, den overføres kun.
Definition af entalpi
Definition af entalpi
**Entalpi **(H ) er den termodynamiske funktion, der beskriver varmestrømning og udtrykkes i kJ/mol. Det er vigtigt at bemærke, at entalpi ikke udelukkende er et mål for varme, men er relateret til tryk og volumen, som du kan se i formlen nedenfor.
dannelsens entalpi er forskellen i entalpi mellem en forbindelse og de grundstoffer, den er lavet af.
Formel for entalpi
Formel for entalpi
H =E + pV
H =entalpi, E =energi, p =tryk, V =volumen
**Første lov om termodynamik ** siger, at energien i et system plus dets omgivelser forbliver konstant og er summen af varmen (q ) og værket (w ), der finder sted i det system.
ΔE =q + w
Arbejde er også en strøm af energi mellem et system og dets omgivelser. En nem måde at visualisere arbejde som en energioverførsel er at forestille sig stempler, der bevæger sig, når der udøves en kraft på dem.
**Hess lov:** Når der er to eller flere afbalancerede kemiske ligninger til at vise trinene i en reaktion, er ændringen i entalpien for nettoligningen er summen af ændringen i entalpier for hver enkelt ligning.
Dette understøtter det faktum, at entalpi er en tilstandsfunktion, hvilket betyder, at den valgte vej ikke påvirker slutresultatet med hensyn til måling af entalpi. Dette er i overensstemmelse med loven om energibevarelse, hvor energi hverken skabes eller ødelægges.
Når stoffer skifter mellem faser (fast, flydende, gas) kan energioverførslen beskrives med følgende formel:
**_q =nCm** Δ_**T **
q =varme, n =mol, C_m =molær varmekapacitet, Δ_T = ændring i temperatur
Specifik varmekapacitet =mængden af energi, der kræves for at hæve temperaturen på 1 kg materiale med 1 grad Celsius
Molær specifik varmekapacitet =mængden af energi, der kræves for at hæve temperaturen på 1 mol materiale med 1 enhed
Beregning af reaktionsentalpi
Beregning af reaktionsentalpi
**Eksempel 1:** Beregn temperaturændringen, der er resultatet af tilføjelse af 250 J termisk energi til 0,50 mol kviksølv.
Visualiser diagrammet over varmesystemet og omgivelserne med pilens retning ind i systemet.
Brug formlen:_q =nCmΔT_
Da du bliver bedt om ændringen i temperatur, omarrangerer du formlen:
ΔT =q/nCm
Slå kviksølvs molære varmekapacitet op:28,3 J/mol K
ΔT =250 J/(s.50 mol)(28,3 J/mol K)
ΔT =17,7 K
dannelsens entalpi
dannelsens entalpi
Beregning af dannelsens entalpi involverer at skrive afbalancerede kemiske ligninger og kombinere ændringen i entalpien for hvert trin. Du skal reducere ligningerne på en sådan måde, at du løser for et enkelt atom af det atom, der er angivet i spørgsmålet. Processen er veldefineret i eksemplet nedenfor.
Beregning af dannelsens entalpi
Beregning af dannelsens entalpi
**Eksempel 2:** Beregn entalpiændringen pr. mol carbonmonoxid for omsætningen af carbonmonoxid med oxygen for at give carbondioxid.
Kulstof forbrændt med begrænset oxygen vil resultere i kulilte (CO), men når der er tilstrækkelig oxygen, vil produktet være kuldioxid (CO2).
2 C (s) –> + O2 (g) –> 2 CO (g)
AH =-221,0 kJ
2 C (s) + O2 (g) –> CO2 (g)
AH =-393,5 kJ
Omarranger den første ligning og vend ΔH, afbalancer derefter den anden ligning.
2 CO 9g) –> 2 C (s) + O2 (g)
ΔH =+221,0 kJ
2 C (s) + 2 O2 (g) –> 2 CO2 (g)
ΔH =(2 mol)(-393,5 kJ) =-787,0 kJ
Annuller '2 C (s)' og 'O2' fra højre side af den første ligning med ækvivalenterne på venstre side af den anden ligning for at opnå følgende:
2 CO (g) + O2 (g) –> 2 CO2 (g)
ΔH =(221,0 kJ) + (-787,0 kJ) =-566,0 kJ
Da ligningen beder om 1 mol CO2, ikke 2, skal du dividere alle dele af ligningen med 2 for at opnå dette.
CO (g) + 1/2 O2 (g) –> CO2 (g)
AH =-566,0 kJ/2 =-283,0 kJ
Metoder til måling af entalpi
Metoder til måling af entalpi
Kalorimetri er den videnskabelige måling af varmeoverførsel fra et system til omgivelser eller omvendt. Der er to typer kalorimetre; den ene hvor trykket forbliver konstant og den anden hvor trykket kan ændre sig. I et system med konstant tryk, hvis der er en volumenændring, er der sket ekspansionsarbejde. Et scenarie, hvor dette kan forekomme, er, når en kemisk proces involverer gasser.
Sidste artikelSådan laves whiteboards:Fra design til produktion
Næste artikelPræcis test af ethanolindhold:En praktisk vejledning
 Varme artikler
Varme artikler
-
 Forskere udvikler de første lægemiddellignende forbindelser til at hæmme undvigende kræftforbund…Kredit:CC0 Public Domain Et team af forskere fra University of Michigan Rogel Cancer Center har udviklet de første lægemiddellignende forbindelser til at hæmme en nøglefamilie af enzymer, hvis fun
Forskere udvikler de første lægemiddellignende forbindelser til at hæmme undvigende kræftforbund…Kredit:CC0 Public Domain Et team af forskere fra University of Michigan Rogel Cancer Center har udviklet de første lægemiddellignende forbindelser til at hæmme en nøglefamilie af enzymer, hvis fun -
 Undersøgelse identificerer æteriske olieforbindelser, der er mest giftige for væggelusKredit:Charles Rondeau/public domain De syntetiske pesticider, der bruges til at bekæmpe væggelusangreb, står over for to problemer:insekterne får en tolerance over for dem, og mange forbrugere le
Undersøgelse identificerer æteriske olieforbindelser, der er mest giftige for væggelusKredit:Charles Rondeau/public domain De syntetiske pesticider, der bruges til at bekæmpe væggelusangreb, står over for to problemer:insekterne får en tolerance over for dem, og mange forbrugere le -
 Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v
Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v -
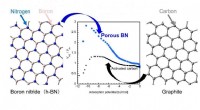 Fange gasser bedre med bornitrid-nanoporerSkematisk illustration af bornitrid- og kulstofstrukturer og adsorptionsevne på porøse bornitrid- og kulstofmaterialer. Kredit:2021 Takahiro Ohkubo Hvad er fælles mellem en teknologi til lagring a
Fange gasser bedre med bornitrid-nanoporerSkematisk illustration af bornitrid- og kulstofstrukturer og adsorptionsevne på porøse bornitrid- og kulstofmaterialer. Kredit:2021 Takahiro Ohkubo Hvad er fælles mellem en teknologi til lagring a
- Hvad betyder CnH2nOn formel?
- Nyopdagede dybhavsmikroer drikker drivhusgasser og måske olieudslip, også
- Lovende resultater opnået med en ny elektrokatalysator, der reducerer behovet for platin
- Hvordan kan to coumpounds lavet af det samme element være så anderledes?
- I hvilken del af blomster produceres pollen?
- Nøgleforskelle mellem ioniske og kovalente forbindelser


