Protoner i organisk kemi:rolle, surhed og basiskhed
1. Syrlighed og basicitet:
* Protonoverførsel: Protoner er centrale i begrebet surhed og basicitet. Syrer donerer protoner, mens baser accepterer dem. Bevægelsen af protoner mellem molekyler bestemmer surheden eller basiciteten af en forbindelse.
* pH-skala: pH-skalaen, der måler surhedsgraden eller alkaliniteten af en opløsning, er baseret på koncentrationen af protoner (H+) i opløsningen.
2. Reaktionsmekanismer:
* Elektrofilt angreb: Mange organiske reaktioner involverer elektrofilt angreb, hvor en elektronmangel art (elektrofil) tiltrækkes af et elektronrigt center. Protoner kan fungere som elektrofiler, der deltager i reaktioner som protonering af alkener eller alkyner.
* Nukleofilt angreb: Ved nukleofilt angreb angriber en nukleofil (elektronrig art) en elektrofil. Protoner kan påvirke nukleofilers reaktivitet, hvilket påvirker deres evne til at angribe.
* Elimineringsreaktioner: Nogle reaktioner involverer fjernelse af en proton og en afgangsgruppe fra et molekyle, hvilket fører til dannelsen af en dobbelt- eller tredobbeltbinding. Protoner er essentielle for disse eliminationsreaktioner.
3. Spektroskopi:
* Kernemagnetisk resonans (NMR) spektroskopi: Protoner har et nukleart spin og er følsomme over for magnetfeltet. NMR-spektroskopi bruger denne egenskab til at skelne mellem forskellige typer protoner i et molekyle, hvilket giver værdifuld information om molekylets struktur.
4. Katalyse:
* Syrekatalyse: Protoner kan fungere som katalysatorer, fremskynde reaktioner ved at lette dannelsen af mellemprodukter eller sænke aktiveringsenergien. Mange organiske reaktioner katalyseres af syrer.
5. Struktur og binding:
* Brintbinding: Protoner deltager i hydrogenbinding, en type intermolekylær interaktion, der er afgørende for egenskaberne af mange organiske molekyler. Denne interaktion er ansvarlig for vandets høje kogepunkt og stabiliteten af DNA.
Eksempler:
* Syre-base-reaktioner: Reaktionen af en stærk syre (som HCl) med vand genererer protoner (H+). Disse protoner reagerer med vandmolekyler, hvilket fører til dannelsen af hydroniumioner (H3O+), hvilket gør opløsningen sur.
* Elektrofil tilføjelse: Tilsætningen af HBr til en alken involverer protoneringen af alkenen, hvilket danner et carbocation-mellemprodukt.
* NMR-spektroskopi: I NMR-spektret af ethanol (CH3CH2OH) optræder protonerne i methylgruppen (CH3) ved et andet kemisk skift end protonerne i methylengruppen (CH2). Denne forskel hjælper med at identificere de forskellige typer protoner i molekylet.
Som konklusion spiller protoner en mangefacetteret og uundværlig rolle i organisk kemi, idet de påvirker reaktioner, spektroskopi og molekylers struktur. At forstå deres adfærd er afgørende for at forstå og forudsige organiske forbindelsers egenskaber og reaktioner.
 Varme artikler
Varme artikler
-
 Brug af elektricitet til at give kemi et løftUD-forskere har udviklet en ny metode til fremstilling af jernbaserede metalorganiske rammer (MOF) materialer. På billedet:Kandidatstuderende Amanda Weaver (til venstre) sætter gang i den UD-udviklede
Brug af elektricitet til at give kemi et løftUD-forskere har udviklet en ny metode til fremstilling af jernbaserede metalorganiske rammer (MOF) materialer. På billedet:Kandidatstuderende Amanda Weaver (til venstre) sætter gang i den UD-udviklede -
 At se nærmere på genetiske skift i kræftEn krystalstruktur af en del af menneskelig DPF2, et protein, der styrer en genetisk switch, der fortæller blodstamceller, hvornår de skal blive røde og hvide blodlegemer. Orange og gule områder illus
At se nærmere på genetiske skift i kræftEn krystalstruktur af en del af menneskelig DPF2, et protein, der styrer en genetisk switch, der fortæller blodstamceller, hvornår de skal blive røde og hvide blodlegemer. Orange og gule områder illus -
 Forskere udvikler superhurtig opladning, højkapacitets kaliumbatterierKredit:CC0 Public Domain Skoltech-forskere i samarbejde med forskere fra Institute for Problems of Chemical Physics af RAS og Ural Federal University har vist, at høj kapacitet, højeffektbatterier
Forskere udvikler superhurtig opladning, højkapacitets kaliumbatterierKredit:CC0 Public Domain Skoltech-forskere i samarbejde med forskere fra Institute for Problems of Chemical Physics af RAS og Ural Federal University har vist, at høj kapacitet, højeffektbatterier -
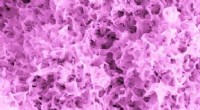 Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha
Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha
- En skjult mangfoldighed af en halv milliard år gamle mikroskopiske dyrefossiler
- Hvor homolog struktur, der ikke involverer lemmerne af hvirveldyr?
- Hvorfor er natriumhydroxid en stærk base?
- Forskere designer molekyler, der hæmmer enzymer i infektionssygdomme
- Dataanalyse kan udløse ny skifergasrevolution
- Hvad er deltaet af fotosynteseaktionen?


