Elektrolyse af NaCl:Hvorfor natriumekstraktion ikke er mulig
* Elektrolyse af vand: Når du elektrolyserer en vandig opløsning, er der også vandmolekyler til stede. Vand reduceres lettere end natriumioner (Na+). Det betyder, at der ved katoden (negativ elektrode), hvor der sker reduktion, produceres brintgas (H2) i stedet for natriummetal.
* Danning af klorgas: Ved anoden (positiv elektrode), hvor der sker oxidation, oxideres chloridioner (Cl-) til dannelse af klorgas (Cl2).
Oversigt over reaktioner:
* Katode (reduktion): 2H2O(l) + 2e- → H2(g) + 2OH-(vandig)
* Anode (oxidation): 2Cl-(vandig) → Cl2(g) + 2e-
For at udvinde natriummetal skal du bruge en anden metode:
* Elektrolyse af smeltet natriumchlorid: Natriummetal kan udvindes ved at elektrolysere smeltet natriumchlorid (NaCl). I dette tilfælde betyder fraværet af vand, at natriumioner er den lettest reducerede art ved katoden, hvilket muliggør dannelsen af natriummetal.
Sig til, hvis du har andre spørgsmål!
Sidste artikelDe hotteste stoffer i universet:et videnskabeligt overblik
Næste artikelFosfor- og klorbinding:Ionisk vs. kovalent
 Varme artikler
Varme artikler
-
 Filtrering af væsker med væsker sparer strømKredit:CC0 Public Domain Filtrering og behandling af vand, både til konsum og til at rense industrielt og kommunalt spildevand, tegner sig for omkring 13 % af al elektricitet, der forbruges i USA
Filtrering af væsker med væsker sparer strømKredit:CC0 Public Domain Filtrering og behandling af vand, både til konsum og til at rense industrielt og kommunalt spildevand, tegner sig for omkring 13 % af al elektricitet, der forbruges i USA -
 Smeltende glas fra usmeltelige forbindelserVahid Nozari ved University of Jena bruger et mikroskop til at undersøge det nye syntetiske glas, som består af en ikke-smeltbar metal-organisk rammeforbindelse (MOF). Kredit:Jens Meyer/University of
Smeltende glas fra usmeltelige forbindelserVahid Nozari ved University of Jena bruger et mikroskop til at undersøge det nye syntetiske glas, som består af en ikke-smeltbar metal-organisk rammeforbindelse (MOF). Kredit:Jens Meyer/University of -
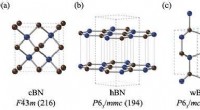 Forudsigelse af den mest stabile bornitridstruktur med kvantesimuleringerStrukturerne og rumgrupperne af (a) zink-blende bornitrid (cBN), (b) hexagonal bornitrid (hBN), (c) wurtzite bornitrid (wBN) og (d) romboedral bornitrid (rBN). Bor- og nitrogenatomer er afbildet i hen
Forudsigelse af den mest stabile bornitridstruktur med kvantesimuleringerStrukturerne og rumgrupperne af (a) zink-blende bornitrid (cBN), (b) hexagonal bornitrid (hBN), (c) wurtzite bornitrid (wBN) og (d) romboedral bornitrid (rBN). Bor- og nitrogenatomer er afbildet i hen -
 Hvad er en vandig opløsning? Et klart overblikSinhyu/iStock/GettyImages En vandig opløsning er en blanding, hvori vand tjener som opløsningsmiddel og opløser et eller flere opløste stoffer. Mens vand oftest forekommer som en væske ved stuetemper
Hvad er en vandig opløsning? Et klart overblikSinhyu/iStock/GettyImages En vandig opløsning er en blanding, hvori vand tjener som opløsningsmiddel og opløser et eller flere opløste stoffer. Mens vand oftest forekommer som en væske ved stuetemper
- Beskyttelse af ribosomgener for at forhindre aldring
- Nye slangearter gemmer sig i almindeligt syn
- Hvad er transformationen af en eksisterende klippe på grund af høj varme og pres?
- Hvilke klipper dannes af hurtig køling af magma?
- Er Nepal og Florida på den samme breddegrad?
- CERN giver grønt lys til at bygge nyt eksperiment til at søge efter ukendte partikler


