Bevaringslove i kemiske ligninger:Atomer og ladning
* Atomer: Antallet af atomer af hvert grundstof på reaktanternes side (venstre side) skal svare til antallet af atomer af det samme grundstof på produkternes side (højre side). Dette følger loven om bevarelse af masse, som siger, at stof ikke kan skabes eller ødelægges i en kemisk reaktion.
* Debitering: I ioniske reaktioner skal den samlede ladning på begge sider af ligningen balanceres. Dette sikrer, at nettoladningen forbliver konstant under hele reaktionen.
Her er grunden til, at det er vigtigt at afbalancere kemiske ligninger:
* Nøjagtig gengivelse af kemiske reaktioner: Balancerede ligninger repræsenterer nøjagtigt forholdet mellem reaktanter og produkter involveret i en kemisk reaktion.
* Stökiometriberegninger: Balancerede ligninger er afgørende for at udføre støkiometriske beregninger, som giver os mulighed for at bestemme mængden af reaktanter og produkter involveret i en reaktion.
* Forståelse af kemiske processer: Ved at afbalancere ligninger får vi en dybere forståelse af, hvordan atomer omarrangeres under kemiske reaktioner.
For eksempel:
Den ubalancerede ligning for forbrænding af metan er:
CH4 + O2 → CO2 + H2O
Den balancerede ligning er:
CH4 + 2O2 → CO2 + 2H2O
Her ser vi at:
* Der er 1 carbonatom, 4 hydrogenatomer og 4 oxygenatomer på begge sider af ligningen, hvilket sikrer bevarelse af atomer.
* Nettoladningen på begge sider er nul, da der ikke er nogen ioner involveret i denne reaktion.
 Varme artikler
Varme artikler
-
 SpaceMat:Graphenes svar på genbrug af dækgummi, der lanceres på markedetKredit:University of Manchester En nystartet virksomhed i Greater Manchester har lanceret det første af en række produkter, der har til formål at reducere spild fra køretøjsdæk, støttet af Graphen
SpaceMat:Graphenes svar på genbrug af dækgummi, der lanceres på markedetKredit:University of Manchester En nystartet virksomhed i Greater Manchester har lanceret det første af en række produkter, der har til formål at reducere spild fra køretøjsdæk, støttet af Graphen -
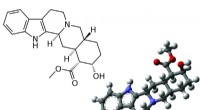 At finde ud af molekylernes 3D-form med et tryk på en knapEt computerprogram kan finde ud af 3D-strukturen (til højre) af molekyler som Yohimbine med et tryk på en knap. Molekyler med den samme 2-D struktur (venstre) kan have forskellige 3-D strukturer. Kred
At finde ud af molekylernes 3D-form med et tryk på en knapEt computerprogram kan finde ud af 3D-strukturen (til højre) af molekyler som Yohimbine med et tryk på en knap. Molekyler med den samme 2-D struktur (venstre) kan have forskellige 3-D strukturer. Kred -
 Stimulering af følesansen med kemiBlot ved berøring kan folk skelne mellem overflader kun baseret på mindre kemiske forskelle. Kredit:Charles Dhong Vores øjne kan være vinduer på verden, men vores fingerspidser sætter os i kontakt
Stimulering af følesansen med kemiBlot ved berøring kan folk skelne mellem overflader kun baseret på mindre kemiske forskelle. Kredit:Charles Dhong Vores øjne kan være vinduer på verden, men vores fingerspidser sætter os i kontakt -
 Forskere kaster lys over nyt billigt materiale til at se i mørketDr. Wendy Sarney bruger den molekylære stråleepitaximaskine ved US Army Research Laboratory til at producere infrarøde detektormaterialer med en ny synteseproces. Kredit:US Army Forskere ved U.S.
Forskere kaster lys over nyt billigt materiale til at se i mørketDr. Wendy Sarney bruger den molekylære stråleepitaximaskine ved US Army Research Laboratory til at producere infrarøde detektormaterialer med en ny synteseproces. Kredit:US Army Forskere ved U.S.
- Hvad kaldes alternative mutationsformer af ethvert gen?
- Hvilke videnskabelige eksperimenter blev udført i rummet?
- Beregn den molære opløselighed af AGBR i en 3,0 x 10-2 m sølvnitrat AgnO3-opløsning?
- NASAs Webb for at udforske en nabo, støvet planetsystem
- Forskere finder en simpel nøgle til risikoen for alvorlige tørvebrande
- Ioniske vs. kovalente bindinger i calciumhydroxid (Ca(OH)₂)


