Oxygen påkrævet til benzenforbrænding:En trinvis beregning
1. Afbalanceret kemisk ligning:
Forbrændingen af benzen (C₆H6) producerer kuldioxid (CO₂) og vand (H₂O):
2 C₆H6 + 15 O₂ → 12 CO₂ + 6 H₂O
2. Beregn mol benzen:
* Molær masse af benzen (C₆H6) =78,11 g/mol
* Mol benzen =(39 g) / (78,11 g/mol) =0,5 mol
3. Bestem påkrævede mol af ilt:
* Fra den afbalancerede ligning kræver 2 mol benzen 15 mol ilt.
* Mol ilt nødvendigt =(0,5 mol benzen) * (15 mol O₂ / 2 mol benzen) =3,75 mol O₂
4. Konverter mol ilt til liter ved STP:
* Ved standard temperatur og tryk (STP) fylder 1 mol af enhver ideel gas 22,4 liter.
* Liter ilt =(3,75 mol O₂) * (22,4 L/mol) =84 liter
Derfor kræves der ca. 84 liter ilt til forbrænding af 39 gram flydende benzen ved STP.
Sidste artikelKaliumacetatsyntese:kemisk ligning og proces
Næste artikelForståelse af aniondannelse:Hvorfor ikke-metaller får elektroner
 Varme artikler
Varme artikler
-
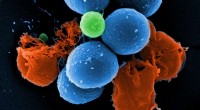 Modificeret kræftlægemiddel effektivt mod multiresistente bakterierScanningselektronmikrografi af intakt MRSA (blå), PK150-induceret vesikeldannelse (grøn), og MRSA ødelagt af PK150 (rød). Kredit:Manfred Rohde / HZI Antibiotika-resistente bakterier er i stigende
Modificeret kræftlægemiddel effektivt mod multiresistente bakterierScanningselektronmikrografi af intakt MRSA (blå), PK150-induceret vesikeldannelse (grøn), og MRSA ødelagt af PK150 (rød). Kredit:Manfred Rohde / HZI Antibiotika-resistente bakterier er i stigende -
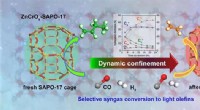 Dynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonverteringDynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonvertering. Kredit:Wang Haodi og Jiao Feng Et forskerhold ledet af prof. Pan Xiulian og prof. Bao Xinhe fra Dalian Institute
Dynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonverteringDynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonvertering. Kredit:Wang Haodi og Jiao Feng Et forskerhold ledet af prof. Pan Xiulian og prof. Bao Xinhe fra Dalian Institute -
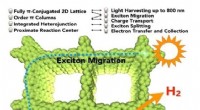 Fotokatalytisk brintproduktion fra vandIllustration af den kulstof-konjugerede kovalente organiske ramme (COF), der viser det fotokatalytiske system, hvor en lang række synligt lys kan høstes til produktion af hydrogengas fra vand. Nanopar
Fotokatalytisk brintproduktion fra vandIllustration af den kulstof-konjugerede kovalente organiske ramme (COF), der viser det fotokatalytiske system, hvor en lang række synligt lys kan høstes til produktion af hydrogengas fra vand. Nanopar -
 Legeringer fra laserprinterenDisse små prøver er lavet af oxiddispersion-forstærkede titaniumaluminider og er blevet lavet som en del af ph.d.-arbejdet. Kredit:Empa I fremtiden, nye designerlegeringer til rumfartsapplikatione
Legeringer fra laserprinterenDisse små prøver er lavet af oxiddispersion-forstærkede titaniumaluminider og er blevet lavet som en del af ph.d.-arbejdet. Kredit:Empa I fremtiden, nye designerlegeringer til rumfartsapplikatione
- Hvad kalder du en bunke sten eller jord?
- Hvad ligger nedenunder:Rødder som drivere af det sydafrikanske landskabsmønster
- Hvad er en god løsning til at opløse rust eller korrosion?
- Hvis et molekyle lugter Minty, hvad kan du hvad kan sige om dens kemi?
- Er det muligt, at acceleration på et øjeblik ikke afhænger af dens hastighedsinstans?
- Hvorfor bruges solvarmeopsamlere til at fange energi fra solen?


