Forståelse af aniondannelse:Hvorfor ikke-metaller får elektroner
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding. Ikke-metaller har generelt højere elektronegativitet end metaller.
* Obligationsdannelse: Når et ikke-metalatom interagerer med et metalatom, trækker ikke-metallets stærkere tiltrækning til elektroner de delte elektroner tættere på sig selv.
* Elektronoverførsel: Denne ubalance i elektrondeling overfører effektivt en elektron fra metalatomet til ikke-metalatomet.
* Danning af ioner:
* Metal: Taber en elektron og bliver til en positivt ladet ion (kation).
* Ikke-metal: Får en elektron og bliver til en negativt ladet ion (anion).
Eksempel: Overvej dannelsen af natriumchlorid (NaCl):
* Natrium (Na): Et metal med lav elektronegativitet.
* Klor (Cl): Et ikke-metal med høj elektronegativitet.
Når natrium og klor reagerer, tiltrækker klor det delte elektronpar stærkere og trækker effektivt en elektron fra natrium. Dette efterlader natrium med en positiv ladning (Na+) og chlor med en negativ ladning (Cl-), hvilket danner den ioniske forbindelse natriumchlorid.
Opsummering: Ikke-metaller har tendens til at få elektroner for at opnå en stabil elektronkonfiguration, hvorfor de danner anioner, når de reagerer med metaller.
 Varme artikler
Varme artikler
-
 Filmfotosensibilisator:Meget effektiv singlet-iltgenerering(a) Fotos af kolonidannende enheder (CFU) for S. aureus inkuberet på LW-PBI-baserede film under bestråling med hvidt lys (90 mW/cm2, 10 min). (b) Absorbansplot registreret ved 291 nm af UA-opløsningen
Filmfotosensibilisator:Meget effektiv singlet-iltgenerering(a) Fotos af kolonidannende enheder (CFU) for S. aureus inkuberet på LW-PBI-baserede film under bestråling med hvidt lys (90 mW/cm2, 10 min). (b) Absorbansplot registreret ved 291 nm af UA-opløsningen -
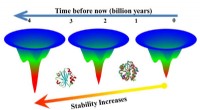 Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv
Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv -
 C. elegans rundorme høster et vigtigt coenzym fra de bakterier, de indtagerCaenorhabditis elegans. Kredit:Wikipedia En undersøgelse udført i C. elegans nematode rundorm kan føre til forbedret behandling af en sjælden menneskelig genetisk lidelse, der forårsager alvorli
C. elegans rundorme høster et vigtigt coenzym fra de bakterier, de indtagerCaenorhabditis elegans. Kredit:Wikipedia En undersøgelse udført i C. elegans nematode rundorm kan føre til forbedret behandling af en sjælden menneskelig genetisk lidelse, der forårsager alvorli -
 Mestring af støkiometri:En trin-for-trin guide til nøjagtige beregningerAf Jack Brubaker – Opdateret 30. august 2022 Støkiometri beskriver de kvantitative forhold mellem reaktanter og produkter i en kemisk reaktion. Selvom konceptet er grundlæggende for kemi, kæmper mang
Mestring af støkiometri:En trin-for-trin guide til nøjagtige beregningerAf Jack Brubaker – Opdateret 30. august 2022 Støkiometri beskriver de kvantitative forhold mellem reaktanter og produkter i en kemisk reaktion. Selvom konceptet er grundlæggende for kemi, kæmper mang


