Beregn HCl-molaritet ud fra pH:En trin-for-trin guide
Forstå forholdet
* pH og [H+] :pH er et mål for hydrogenionkoncentrationen ([H+]) i en opløsning. Forholdet er:
pH =-log[H+]
* HCl er en stærk syre :Det betyder, at det dissocierer fuldstændigt i vand, hvilket betyder, at hvert HCl-molekyle producerer en H+-ion.
Beregninger
1. Find [H+] :
* Omarranger pH-ligningen:[H+] =10^(-pH)
* Erstat den givne pH:[H+] =10^(-5,7) =2,0 x 10^(-6) M
2. Molaritet af HCl :Da HCl dissocierer fuldstændigt, er molariteten af HCl lig med [H+]:
* Molaritet af HCl =2,0 x 10^(-6) M
Derfor er molariteten af HCl-opløsningen med en pH-værdi på 5,7 2,0 x 10^(-6) M.
 Varme artikler
Varme artikler
-
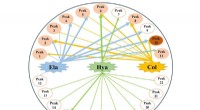 Potentielle anti-aldringskomponenter af Moringa oleifera bladNetværksdiagram over multikomponent- og multi-target-interaktioner af Moringa oleifera-blade. Kredit:WBG Moringa oleifera Lam., også kendt som Miracle Tree, primært afledt fra Indien, er nu vidt ud
Potentielle anti-aldringskomponenter af Moringa oleifera bladNetværksdiagram over multikomponent- og multi-target-interaktioner af Moringa oleifera-blade. Kredit:WBG Moringa oleifera Lam., også kendt som Miracle Tree, primært afledt fra Indien, er nu vidt ud -
 Forskere udvikler 3-D printsubstrat med dynamiske bindinger til justerbare egenskaber4-D-print:En farve- og formskiftende blomst i mikrostørrelse skabt ved direkte laserskrivning. Kredit:TU/e Fantastiske former kan laves ved hjælp af 3-D print, men til mange applikationer skal det
Forskere udvikler 3-D printsubstrat med dynamiske bindinger til justerbare egenskaber4-D-print:En farve- og formskiftende blomst i mikrostørrelse skabt ved direkte laserskrivning. Kredit:TU/e Fantastiske former kan laves ved hjælp af 3-D print, men til mange applikationer skal det -
 Kemikere syntetiserer psykotrope forbindelser fra regnskovstræKredit:Scripps Research Institute Barken fra Galbulimima belgraveana-træet, der kun findes i fjerntliggende regnskove i Papua Ny Guinea og det nordlige Australien, har længe været brugt af oprindel
Kemikere syntetiserer psykotrope forbindelser fra regnskovstræKredit:Scripps Research Institute Barken fra Galbulimima belgraveana-træet, der kun findes i fjerntliggende regnskove i Papua Ny Guinea og det nordlige Australien, har længe været brugt af oprindel -
 Transformering af kuldioxid – forskere udvikler ny to-trins CO2-konverteringsteknologiUD Professor Feng Jiaos team konstruerede en elektrolysator, afbilledet her, at gennemføre deres nye to-trins konverteringsproces. Kredit:Feng Jiao Et team af forskere ved University of Delawares
Transformering af kuldioxid – forskere udvikler ny to-trins CO2-konverteringsteknologiUD Professor Feng Jiaos team konstruerede en elektrolysator, afbilledet her, at gennemføre deres nye to-trins konverteringsproces. Kredit:Feng Jiao Et team af forskere ved University of Delawares
- Når ok ikke er ok:Sikkerhedspræsentant taler om syntetiske klik
- Hvad er solmængder?
- Hvilke former for energi har en bevægelig bil?
- Succesfuld syntese af nanomateriale, der forbedrer katalysatorens effektivitet
- Hvad er den konnotative betydning af former jord ved Abiquiu?
- Hvad er massenummeret for et atom?


