Molalitet:Forstå mol af opløst stof pr. kilo opløsningsmiddel
Her er en opdeling:
* Molalitet (m): Koncentrationen af en opløsning udtrykt som antallet af mol opløst stof pr. kg opløsningsmiddel.
* Løsning: Stoffet, der er ved at blive opløst.
* Opløsningsmiddel: Stoffet, der opløser det opløste stof.
Eksempel:
En opløsning indeholdende 0,5 mol glucose opløst i 1 kg vand har en molalitet på 0,5 m.
Hvorfor bruge molalitet?
* Uafhængig af temperatur: Molalitet er uafhængig af temperaturændringer, fordi den er baseret på masse, som ikke ændres med temperaturen.
* Nyttig til kolligative egenskaber: Molalitet bruges til at beregne kolligative egenskaber som frysepunktsnedsættelse og kogepunktsforhøjelse, som er relateret til koncentrationen af opløste partikler i en opløsning.
Nøgleforskel fra molaritet:
* Molaritet (M): Mol opløst stof pr. liter *opløsning* (opløst stof + opløsningsmiddel). Molariteten er afhængig af temperaturen, da volumen ændres med temperaturen.
 Varme artikler
Varme artikler
-
 Polymerer bliver fanget af kærlighed-hadkemi af olie og vandForskere ved Oak Ridge National Laboratory og University of Tennessee sporede polymerselvsamling ved væske-væske-grænsefladen i realtid. Kredit:Michelle Lehman/Oak Ridge National Laboratory, US Depart
Polymerer bliver fanget af kærlighed-hadkemi af olie og vandForskere ved Oak Ridge National Laboratory og University of Tennessee sporede polymerselvsamling ved væske-væske-grænsefladen i realtid. Kredit:Michelle Lehman/Oak Ridge National Laboratory, US Depart -
 ROSINA spektrale målinger vækker komets kemi til liveArbejdshestinstrument ROSINA-DFMS (Rosetta Orbiter Sensor til Ion- og Neutral Analysis-Double Focusing Mass Spectrometer). Kredit:University of Bern Lanceret marts 2004 og efter en 10-årig rejse o
ROSINA spektrale målinger vækker komets kemi til liveArbejdshestinstrument ROSINA-DFMS (Rosetta Orbiter Sensor til Ion- og Neutral Analysis-Double Focusing Mass Spectrometer). Kredit:University of Bern Lanceret marts 2004 og efter en 10-årig rejse o -
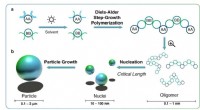 Serendipitous baggårdseksperiment kaster lys over produktion af polymererPrincip for lysinduceret partikeldannelse. a Under bestråling danner en AA-monomer et reaktivt mellemprodukt, som reagerer med en BB-monomer i en Diels-Alder-trinvækstpolymerisation. b Når de lineære
Serendipitous baggårdseksperiment kaster lys over produktion af polymererPrincip for lysinduceret partikeldannelse. a Under bestråling danner en AA-monomer et reaktivt mellemprodukt, som reagerer med en BB-monomer i en Diels-Alder-trinvækstpolymerisation. b Når de lineære -
 Biofunktionaliseret keramik til reparation af kranieknogledefekter - in vivo undersøgelseIllustration af de multifunktionelle materialer eksperimentelt udviklet i undersøgelsen til in vivo anvendelser af celleproliferation og kranioplastik. Defektheling i en gnavermodel observeres efter 1
Biofunktionaliseret keramik til reparation af kranieknogledefekter - in vivo undersøgelseIllustration af de multifunktionelle materialer eksperimentelt udviklet i undersøgelsen til in vivo anvendelser af celleproliferation og kranioplastik. Defektheling i en gnavermodel observeres efter 1
- Hvor mange gram opløste stoffer er et tusind havvand?
- Hvad er grundlaget for videnskabelige forklaringer?
- Hvorfor kaldes geologer geologer?
- Den energi, der strømmer fra en varmere krop til koldere, kaldes?
- Eksperter reagerer på den seneste rapport fra det mellemstatslige panel om klimaændringer
- Hvordan konverterer jeg M3 til kilogram?


