Forståelse af kemiske koncentrationsenheder:Molaritet vs. Molalitet
Her er hvorfor:
* Forskellige enheder udtrykker forskellige aspekter af koncentration:
* Molaritet (mol/L): Udtrykker antallet af mol opløst stof pr. liter opløsning. Dette er meget nyttigt til støkiometriske beregninger og reaktioner.
* Molalitet (mol/kg): Udtrykker antallet af mol opløst stof pr. kg opløsningsmiddel. Dette er temperaturuafhængigt, hvilket gør det nyttigt i situationer, hvor temperaturen ændrer sig betydeligt.
* Masseprocent (% w/w): Udtrykker massen af opløst stof som en procentdel af opløsningens samlede masse. Dette bruges ofte i hverdagsapplikationer, såsom fødevaremærkning.
* Volumenprocent (% v/v): Udtrykker volumen af opløst stof som en procentdel af opløsningens samlede volumen. Dette er nyttigt til blandinger af væsker.
* Parts per million (ppm) og parts per billion (ppb): Udtryk meget lave koncentrationer af opløste stoffer, ofte brugt til sporurenheder og miljøanalyser.
I sidste ende afhænger valget af den bedste koncentrationsenhed af den specifikke situation. Her er nogle vejledende faktorer:
* Løsningens art: Vandige opløsninger bruger ofte molaritet, mens blandinger af væsker kan bruge volumenprocent.
* Formålet med målingen: Støkiometriske beregninger bruger ofte molaritet, mens miljøanalyse kan bruge ppm eller ppb.
* Temperaturafhængigheden: Molalitet foretrækkes, når temperaturændringer forventes.
Det er vigtigt at være bekendt med de forskellige koncentrationsenheder og deres anvendelser for at vælge den mest passende til en given situation.
 Varme artikler
Varme artikler
-
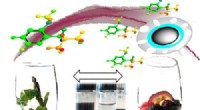 Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel
Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel -
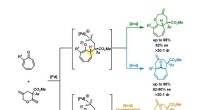 Divergent syntese af bicykliske mellemstore ringstrukturerFigur viser reaktionsvejene for den divergerende syntese af tre klasser af forbindelser. Ved at bruge det samme sæt af udgangsmaterialer og palladiumkatalysator, men udsat for forskellige reaktionsbet
Divergent syntese af bicykliske mellemstore ringstrukturerFigur viser reaktionsvejene for den divergerende syntese af tre klasser af forbindelser. Ved at bruge det samme sæt af udgangsmaterialer og palladiumkatalysator, men udsat for forskellige reaktionsbet -
 Karamelreceptor identificeretDen lugtende furaneol giver jordbær og andre fødevarer en karamellignende aroma. Figur:G. Olias / LSB, Figuren viser jordbær og strukturformlen for lugtstoffet furaneol. Kredit:G. Olias / LSB Hvem
Karamelreceptor identificeretDen lugtende furaneol giver jordbær og andre fødevarer en karamellignende aroma. Figur:G. Olias / LSB, Figuren viser jordbær og strukturformlen for lugtstoffet furaneol. Kredit:G. Olias / LSB Hvem -
 Ny metode tillader nem, alsidig syntese af lactonmolekylerKredit:CC0 Public Domain Kemikere ved Scripps Research har afsløret en metode til at omdanne billige og bredt tilgængelige kemikalier kendt som dicarboxylsyrer til potentielt meget værdifulde molek
Ny metode tillader nem, alsidig syntese af lactonmolekylerKredit:CC0 Public Domain Kemikere ved Scripps Research har afsløret en metode til at omdanne billige og bredt tilgængelige kemikalier kendt som dicarboxylsyrer til potentielt meget værdifulde molek
- Intel:Hot Chips-begivenhedsdetaljer AI-styrke-processorer
- Hvad er en styrke, der bygger op bjerge og landmasser?
- Hvordan hjalp Sir Isaac Newton med den videnskabelige metode?
- Hvad tvangsmæssig dating-app brugere har til fælles
- Massiv protostjerne bliver ved med at vokse på trods af ioniseringsopvarmning med ultraviolet lys
- NASA finder den tropiske cyklon Ann over det store barriererev


