pH-effekter på enzymer:hvordan surhed og alkalinitet påvirker enzymets struktur og funktion
Sure løsninger:
* Denaturering: Syrer kan forstyrre den delikate balance mellem hydrogenbindinger og elektrostatiske interaktioner, der holder enzymets tredimensionelle struktur (dets konformation) sammen. Denne forstyrrelse, kendt som denaturering, ændrer det aktive sted - det specifikke område, hvor enzymet binder til dets substrat. Et denatureret enzym er i det væsentlige ikke-funktionelt.
* Afbrydelse af ioniseringstilstand: Enzymer er ofte afhængige af specifikke ioniseringstilstande af aminosyrerester inden for deres aktive sted. Syrer kan ændre pH i miljøet, ændre ioniseringstilstanden af disse rester, hvilket kan forstyrre substratbinding og katalytisk aktivitet.
Grundlæggende løsninger:
* lignende virkninger som syrer: Selvom de er mindre almindelige, kan meget basale opløsninger også denaturere enzymer ved at forstyrre deres struktur.
* Ioniseringsforstyrrelse: I lighed med sure opløsninger kan baser også ændre ioniseringstilstanden af nøgleaminosyrerester i det aktive sted, hvilket kompromitterer enzymatisk aktivitet.
Optimal pH:
Hvert enzym har et optimalt pH-område, hvor det fungerer mest effektivt. Uden for dette område falder den enzymatiske aktivitet. Dette skyldes de specifikke pH-krav til det aktive sted for at opretholde den korrekte konformation og ioniseringstilstande for optimal substratbinding og katalyse.
Eksempler:
* Pepsin: Dette enzym, der findes i maven, fungerer bedst i et meget surt miljø (pH 2). Denne surhedsgrad er afgørende for dens evne til at nedbryde proteiner.
* Trypsin: Dette enzym, der findes i tyndtarmen, fungerer optimalt ved en let alkalisk pH (omkring 8).
Konsekvenser af pH-ændringer:
* Reduceret aktivitet: Enzymer uden for deres optimale pH-område kan have nedsat aktivitet, bremse eller standse reaktioner.
* Fuldstændig inaktivering: Ekstreme pH-ændringer kan føre til irreversibel denaturering, hvilket permanent gør enzymet ubrugeligt.
Opsummering:
Både sure og basiske opløsninger kan påvirke enzymmolekyler negativt ved at ændre deres konformation, forstyrre ioniseringstilstanden af kritiske rester og i sidste ende påvirke deres aktivitet. Opretholdelse af den passende pH er essentiel for enzymfunktionen og dermed for mange biologiske processer i levende organismer.
Sidste artikelForståelse af aniondannelse:Hvorfor ikke-metaller får elektroner
Næste artikelMolekylære dipolmomenter:Hvornår annullerer de?
 Varme artikler
Varme artikler
-
 Mestring af konverteringsfaktorer i kemiske formler:En praktisk vejledningI kemi repræsenterer subscripts i formler kvantitative forhold, ikke kun symboler. Hvert subscript koder for en konverteringsfaktor, der forbinder elementer, molekyler og målbare mængder. At forstå di
Mestring af konverteringsfaktorer i kemiske formler:En praktisk vejledningI kemi repræsenterer subscripts i formler kvantitative forhold, ikke kun symboler. Hvert subscript koder for en konverteringsfaktor, der forbinder elementer, molekyler og målbare mængder. At forstå di -
 Molekylær lim gør perovskite solceller dramatisk mere pålidelige over tidForskere har brugt selvsamlet monolags molekylær lim til at styrke grænseflader i perovskite solceller for at gøre dem mere effektive, stabil og pålidelig. Kredit:Padture lab/Brown University Et f
Molekylær lim gør perovskite solceller dramatisk mere pålidelige over tidForskere har brugt selvsamlet monolags molekylær lim til at styrke grænseflader i perovskite solceller for at gøre dem mere effektive, stabil og pålidelig. Kredit:Padture lab/Brown University Et f -
 Spin-out-virksomhed hjælper med at få effektive lægemidler på markedet, hurtigere og billigereKredit:Swansea University At få bedre stoffer på markedet hurtigere, og til en brøkdel af prisen, er et skridt nærmere takket være teknologi til at fremskynde testprocessen, som udvikles af et spi
Spin-out-virksomhed hjælper med at få effektive lægemidler på markedet, hurtigere og billigereKredit:Swansea University At få bedre stoffer på markedet hurtigere, og til en brøkdel af prisen, er et skridt nærmere takket være teknologi til at fremskynde testprocessen, som udvikles af et spi -
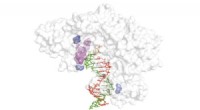 En ny rettet evolutionsteknik til at frigøre potentialet for xeno-nukleinsyrerDiagram, der viser den omvendte transkriptasestruktur (hvid) med spirende cDNA -streng (rød), XNA -skabelon (grøn) og områder kritiske for omvendt transkription af XNA -skabeloner (blå og lilla). Kred
En ny rettet evolutionsteknik til at frigøre potentialet for xeno-nukleinsyrerDiagram, der viser den omvendte transkriptasestruktur (hvid) med spirende cDNA -streng (rød), XNA -skabelon (grøn) og områder kritiske for omvendt transkription af XNA -skabeloner (blå og lilla). Kred
- Hvad er venlige mikrober?
- Ingeniører opfinder smartphone-enhed, der registrerer skadelige alger på 15 minutter
- Renere vand gennem majs
- Hvad forårsager sæsoner? Jordens hældning og kredsløb
- Forskere borer dybt under Atlanten og afdækker et massivt ferskvandsreservoir
- Bekæmpelse af brændbare beklædningsfarer


